题目内容
NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、4.6g组成为C2H6O的有机物,所含C-H键数目一定为0.6NA |
| B、12g金刚石中含有的共价键数为2NA |
| C、0.1mol的白磷(P4)或甲烷中所含的σ键数均为0.4NA |
D、0.5mol雄黄(As4S4结构如图)含有NA个S-S键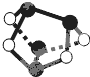 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.该有机物可能是乙醇也可能是乙醚,4.6g该有机物的物质的量是0.1mol,再结合每个分子含有的C-H键数目判断;
B.金刚石中,每个C与其它4个C形成了四个共价键,根据均摊法计算出1molC含有的共价键;
C.白磷分子中含有6个P-P键,甲烷分子中含有4个C-H键;
D.As原子半径比S原子半径大,由结构可知,黑色球为As,白色球为S,分子中不存在S-S键.
B.金刚石中,每个C与其它4个C形成了四个共价键,根据均摊法计算出1molC含有的共价键;
C.白磷分子中含有6个P-P键,甲烷分子中含有4个C-H键;
D.As原子半径比S原子半径大,由结构可知,黑色球为As,白色球为S,分子中不存在S-S键.
解答:
解:A.该有机物可能是乙醇也可能是乙醚,4.6g该有机物的物质的量是0.1mol,如果是乙醇,所含C-H键数目一定为0.5NA,如果是乙醚,含有的C-H键数目一定为0.6NA,如果是乙醇和乙醚的混合物,则含有的C-H键数目介于二者之间,故A错误;
B.12g金刚石中含有1molC,金刚石中,每个C与其它4个C形成了4个共价键,每个碳原子形成的共价键数目为:
×4=2,所以1molC原子形成的共价键为2mol,含有的共价键数目为2NA,故B正确;
C.白磷分子中含有6个P-P键,甲烷分子中含有4个C-H键,0.1mol的白磷(P4)共价键数0.6mol,0.1mol甲烷中所含的共价键数均为0.4NA,故C错误;
D.黑色球为As,白色球为S,雄黄分子中不存在S-S键,故D错误;
故选B.
B.12g金刚石中含有1molC,金刚石中,每个C与其它4个C形成了4个共价键,每个碳原子形成的共价键数目为:
| 1 |
| 2 |
C.白磷分子中含有6个P-P键,甲烷分子中含有4个C-H键,0.1mol的白磷(P4)共价键数0.6mol,0.1mol甲烷中所含的共价键数均为0.4NA,故C错误;
D.黑色球为As,白色球为S,雄黄分子中不存在S-S键,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的综合应用,侧重物质结构与化学键的知识的考查,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确常见物质的空间结构及成键情况,学会均摊法的应用方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
| A、盐酸、天然气、醋酸、干冰 |
| B、胆矾、漂白粉、氯化钾、氯气 |
| C、氯化钠、福尔马林、硫酸钠、乙醇 |
| D、单甘油酯、混甘油酯、苛性钾、石灰 |
根据热化学方程式S(s)+O2(g)═SO2(g)△H=-297.23kJ?mol-1,分析下列说法正确的是( )
| A、S(g)+O2(g)═SO2(g)|△H|=297.23 kJ?mol-1 |
| B、S(g)+O2(g)═SO2(g)|△H|<297.23 kJ?mol-1 |
| C、1 mol SO2(g)所具有的能量大于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
| D、1 mol SO2(g)所具有的能量小于1 mol S(s)与1 mol O2(g)所具有的能量之和 |
下列溶液中微粒的物质的量浓度关系在常温下一定正确的是( )
| A、0.1mol/LNH4Cl溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、pH=2的HCl溶液与pH=12的NaOH溶液等体积混合所得溶液中:c(Na+)=c(Cl-)>c(OH-)=c(H+) |
| C、0.2mol/L NaClO溶液中:c(Na+)=c(HClO)+c(ClO-)+c(OH-) |
| D、0.1mol/L Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |

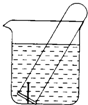 如图水槽中试管内有一枚铁钉,放置数天后观察:
如图水槽中试管内有一枚铁钉,放置数天后观察: