题目内容
13.下列装置都可制取HCl气体,其中药品选用错误的是( )| A. | 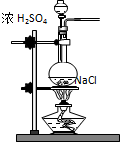 | B. | 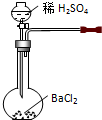 | C. | 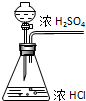 | D. | 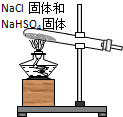 |
分析 HCl易溶于水,制备氯化氢,应用浓硫酸,浓硫酸可与氯化钠、浓盐酸反应,也可用硫酸氢钠和氯化钠在加热条件下制备氯化氢,以此解答该题.
解答 解:A.浓硫酸和氯化钠在加热条件下可生成硫酸钠、氯化氢,可用于制备氯化氢气体,故A正确;
B.稀硫酸和氯化钡反应生成硫酸钡和盐酸,不能得到氯化氢,故B错误;
C.浓硫酸具有吸水性,且溶于水放热,可用浓硫酸和浓盐酸反应制备氯化氢,故C正确;
D.加热条件下硫酸氢钠和氯化钠反应生成氯化氢和硫酸钠,故D正确.
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握气体的制备原理、实验装置的作用、气体的成分为解答的关键,侧重分析与实验能力的考查,注意实验技能应用及实验评价性分析,题目难度不大.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
4.常温下,下列各组离子一定能在指定溶液中大量共存的是( )
| A. | 1.0 mol•L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | |
| B. | $\frac{{K}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液:NH4+、Ca2+、Cl-、NO3- | |
| C. | pH=1的溶液:Al3+、Ag(NH3)2+、Cl-、SO42- | |
| D. | 由水电离产生c(H+)=10-10mol/L的溶液:NH4+、Ca2+、AlO2-、S2- |
8.根据下表信息,判断0.10mol/L的下列各溶液pH值最大的是( )
| 酸 | 电离常数 |
| CH3COOH | Ki=1.8×10 -5 |
| H2CO3 | Ki1=4.3×10 -7,Ki2=5.6×10 -11 |
| H2S | Ki1=9.1×10 -8,Ki2=1.1×10 -12 |
| H3PO4 | Ki1=7.5×10 -3,Ki2=6.2×10 -8,Ki3=2.2×10 -13 |
| A. | CH3COONa | B. | Na2CO3 | C. | Na2S | D. | Na3PO4 |
18.用下列三种装置制备和收集二氧化碳气体:

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )

将收集的三瓶CO2置于天平上称量,若三个集气瓶的体积与质量均相等,称量结果正确的是( )
| A. | ①最重 | B. | ②最重 | C. | ③最重 | D. | ①②③一样重 |
2.下列说法正确的是( )
| A. | 胶体区别于其他分散系的本质特征是胶体可发生丁达尔效应 | |
| B. | 在一定温度和压强下,气体体积主要取决于气体分子之间的平均间距 | |
| C. | 道尔顿、阿伏伽德罗、卢瑟福、波尔等科学家的研究不断更新人们对原子结构的认识 | |
| D. | 确定物质中是否含有C、H、O、N、Cl、Br、S等元素可用元素分析仪,确定物质中是否含有哪些金属元素可用原子吸收光谱 |
19.下列实验操作正确的是( )
| A. | 排水法收集气体后,先熄灭酒精灯,再取出导气管 | |
| B. | 蒸馏自来水时,冷凝水从上口进,从下口出 | |
| C. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| D. | 稀释浓硫酸时,应将浓硫酸慢慢加入水中并及时搅拌 |