题目内容
1.下列化学用语正确的是( )| A. | 乙烯的结构简式:CH2CH2 | B. | 甲烷的结构式CH4 | ||
| C. | 苯的分子式C6H6 | D. | 羟基:OH |
分析 A.乙烯的结构简式中不能省略碳碳双键;
B.结构式中应该用短线表示出所有的共价键;
C.苯分子中含有6个C、6个H原子;
D.羟基正确的结构简式为-OH.
解答 解:A.乙烯分子中含有1个碳碳双键,其正确的结构简式为:CH2=CH2,故A错误;
B.甲烷分子式为CH4,碳原子与氢原子之间形成1对共用电子对,结构式为 ,故B错误;
,故B错误;
C.苯分子中中C、H原子数都是6,其分子式为:C6H6,故C正确;
D.羟基为中性原子团,其结构简式为:-OH,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及结构式、结构简式、分子式等知识,明确常见化学用语的书写原则即可解答,试题有利于提高学生的规范答题能力.

练习册系列答案
相关题目
19.下列实验合理的是( )
| A. | 用溴水除去NaCl溶液中的NaI | |
| B. | 用NaOH溶液与HCl溶液制备NaCl | |
| C. | 用NaOH溶液除去乙酸乙酯中的溴 | |
| D. | 用冷却饱和溶液法提纯含少量NaCl杂质的KNO3 |
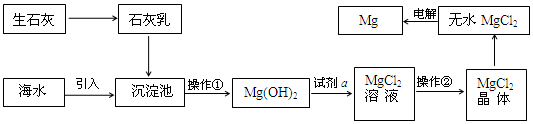
9.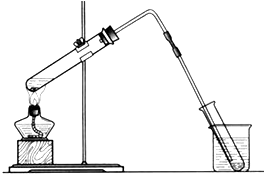 海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.
海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.
(1)如图是用海水制取少量蒸馏水的简易装置,其原理与课本中的实验原理完全相同.装置中使用了较长的玻璃管,其作用是导气兼冷凝,烧杯中还应盛装的物质是冰水.
(2)海带中含有丰富的碘,海带提碘可将海带灼烧、溶解、煮沸、过滤得含I-的滤液,滤液经酸化、氧化得含单质碘的溶液.回答下列问题:
①海带灼烧时用来盛装海带的仪器是坩埚(填仪器名称)
②已知KMnO4、H2O2、Cl2等均可与I-反应生成I2,且KMnO4、H2O2、Cl2对应的生成物分别为Mn2+、H2O、Cl-.从绿色化学的角度看I-转化成I2,最好选H2O2 (上述三种中选择)
(3)海水晒盐得到的盐含有较多的杂质.某学习小组欲设计实验提纯粗盐.
①若只除去其中的不溶性杂质,应经过的实验步骤是溶解、过滤、蒸发.
②若要进一步除去上述粗盐中的可溶性杂质,应选择合理的除杂试剂.请填写表:
③为确保杂质除尽,所加试剂应适当过量.如何判断SO42-是否除尽?取上层清液少许于试管中,滴加BaCl2溶液,若无白色沉淀产生,则SO42-已除尽
④上述除杂试剂加入的先后顺序应满足的一般条件是Na2CO3溶液应加在BaCl2溶液之后
⑤按顺序加入上述除杂试剂过滤后,还应加入适量稀HCl,其目的是除去过量除杂试剂中的OH-和CO32-,,判断加入稀HCl适量的方法可以是向滤液中逐滴滴加稀HCl,调节溶液pH=7.
 海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.
海洋是巨大的资源宝库,从海洋中可获得淡水、单质碘、食盐等物质.(1)如图是用海水制取少量蒸馏水的简易装置,其原理与课本中的实验原理完全相同.装置中使用了较长的玻璃管,其作用是导气兼冷凝,烧杯中还应盛装的物质是冰水.
(2)海带中含有丰富的碘,海带提碘可将海带灼烧、溶解、煮沸、过滤得含I-的滤液,滤液经酸化、氧化得含单质碘的溶液.回答下列问题:
①海带灼烧时用来盛装海带的仪器是坩埚(填仪器名称)
②已知KMnO4、H2O2、Cl2等均可与I-反应生成I2,且KMnO4、H2O2、Cl2对应的生成物分别为Mn2+、H2O、Cl-.从绿色化学的角度看I-转化成I2,最好选H2O2 (上述三种中选择)
(3)海水晒盐得到的盐含有较多的杂质.某学习小组欲设计实验提纯粗盐.
①若只除去其中的不溶性杂质,应经过的实验步骤是溶解、过滤、蒸发.
②若要进一步除去上述粗盐中的可溶性杂质,应选择合理的除杂试剂.请填写表:
| 杂质 | CaCl2 | MgCl2 | Na2SO4 |
| 除杂试剂 |
④上述除杂试剂加入的先后顺序应满足的一般条件是Na2CO3溶液应加在BaCl2溶液之后
⑤按顺序加入上述除杂试剂过滤后,还应加入适量稀HCl,其目的是除去过量除杂试剂中的OH-和CO32-,,判断加入稀HCl适量的方法可以是向滤液中逐滴滴加稀HCl,调节溶液pH=7.
16.下列有关0.1mol•L-1 NaOH 溶液的叙述正确的是( )
| A. | 100mL该溶液中含有Na+0.01mol | |
| B. | 1 L该溶液中含有NaOH40 g | |
| C. | 从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol•L-1 | |
| D. | 在1L水中溶解4g NaOH即可配制得0.1 mol•L-1 NaOH溶液 |
6.下列有关热化学方程式的叙述正确的是( )
| A. | 已知2H2(g)+O2(g)=2H2O(l)△H=-571.6 kJ•mol-1,则氢气的燃烧热为285.8 KJ/mol | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l)△H=-57.4 kJ•mol-1 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
13.在下列实验操作与安全事故处理中错误的是( )
| A. | 使用水银温度计测量烧杯中的水浴温度时,不慎打破水银球,用滴管将水银吸出放入水封的小瓶中,残破的温度计插入装有硫粉的广口瓶中 | |
| B. | 用试管夹从试管底部往上夹住距试管口约$\frac{1}{3}$处,手持试管夹长柄末端,进行加热 | |
| C. | 使用滴管取液时,先将滴管伸入试剂瓶中,然后用手指捏紧橡胶乳头,赶出滴管中的空气,放开手指,试剂即被吸入 | |
| D. | 把玻璃导管插入橡胶塞孔时,用厚布护手,紧握用水湿润的插入端,缓慢旋进塞孔中 |
11.已知:①2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol;
②Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
②Na2O2(s)+CO2(g)=Na2CO3(s)+$\frac{1}{2}$O2(g)△H=-226kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
| A. | CO的燃烧热为 283 kJ | |
| B. | 反应①正反应活化能与逆反应活化能之差为+566 kJ/mol | |
| C. | 反应 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)△H>-452 kJ/mol | |
| D. | CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 6.02×1023 |
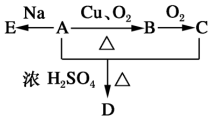 化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化:
化合物A(C4H10O)是一种有机溶剂,A可以发生如图变化: