题目内容
18.目前世界上60%的镁是从海水提取的.海水提镁的主要流程如图: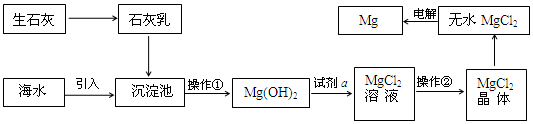
提示:①MgCl2晶体的化学式为MgCl2•6H2O;
②MgO的熔点为2852℃,无水MgCl2的熔点为714℃.
(1)操作①的名称是过滤,操作②的名称蒸发浓缩、冷却(或降温)结晶、过滤.
(2)写出Mg(OH)2和试剂a反应的离子方程式Mg(OH)2+2H+═Mg2++2H2O.
(3)用氯化镁电解生产金属镁的化学方程式为MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;当电子转移为8mol时,理论上产生的氯气在标准状况下的体积为89.6L;写出用氯气生产漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
(4)工业上是将氢氧化镁转变为氯化镁,再电解氯化镁来制取镁单质;而不采用加热Mg(OH)2得到MgO,再电解熔融MgO的方法制金属镁,其原因是MgO熔点很高,熔融时耗费大量的能量而增加生产成本.
分析 生石灰溶于水得到氢氧化钙溶液加入沉淀池,沉淀镁离子过滤,得到氢氧化镁固体,加入稀盐酸后溶解得到氯化镁溶液,通过蒸发浓缩、冷却结晶,过滤洗涤得到氯化镁晶体,熔融电解得到金属镁;
(1)分析流程操作①为过滤,操作②为溶液中得到溶质晶体的方法为蒸发浓缩,冷却结晶,过滤洗涤得到;
(2)试剂a为溶解氢氧化镁得到氯化镁溶液,结合提纯目的得到需要加入盐酸;
(3)电解熔融氯化镁得到金属镁和氯气;结合电子守恒计算生成氯气标准状况下的体积,氯气和石灰乳反应生成氯化钙、次氯酸钙和水得到漂白粉;
(4)氧化镁熔点为2852℃,无水MgCl2的熔点为714℃,MgO熔点很高,熔融时耗费大量的能量而增加生产成本.
解答 解:生石灰溶于水得到氢氧化钙溶液加入沉淀池,沉淀镁离子过滤,得到氢氧化镁固体,加入稀盐酸后溶解得到氯化镁溶液,通过蒸发浓缩、冷却结晶,过滤洗涤得到氯化镁晶体,熔融电解得到金属镁;
(1)分析流程操作①是溶液中分离出固体的方法,操作为过滤,操作②为溶液中得到溶质晶体的方法为蒸发浓缩,冷却结晶,过滤洗涤得到;
故答案为:过滤;蒸发浓缩;冷却结晶;
(2)试剂a为溶解氢氧化镁得到氯化镁溶液,结合提纯目的得到需要加入盐酸,反应的离子方程式为:Mg(OH)2+2H+=Mg2++2H2O,
故答案为:Mg(OH)2+2H+=Mg2++2H2O;
(3)电解熔融氯化镁得到金属镁和氯气,MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,化学方程式中生成1mol氯气电子转移2mol,当电子转移为8mol时,理论上产生的氯气在标准状况下的体积=$\frac{8mol}{2mol}$×1mol×22.4L/mol=89.6L,
用氯气生产漂白粉的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:MgCl2(熔融)$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;89.6L;2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
(4)氧化镁熔点为2852℃,无水MgCl2的熔点为714℃,MgO熔点很高,熔融时耗费大量的能量而增加生产成本,
故答案为:MgO熔点很高,熔融时耗费大量的能量而增加生产成本.
点评 本题考查了物质分离的方法和流程判断,物质性质和实验基本操作是解题关键,题目较简单.

 下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
下面是某化学学习小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.I.课本介绍了乙醇氧化的实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2mL乙醇的试管里,反复操作几次.注意闻生成物的气味,并观察铜丝表面的变化.
(1)小赵同学用化学方法替代“闻生成物的气味”来说明生成物的出现,该化学方法中所另加的试剂及出现的主要现象是银氨溶液,出现银镜或新制氢氧化铜悬浊液,产生砖红色沉淀.(用所学的知识回答)
(2)小赵同学在探究“闻生成物的气味”的替代方法时,偶然发现向溴水中加入足量的乙醛溶液,可以看到溴水褪色.该同学为解释上述现象,提出三种猜想:
①溴与乙醛发生取代反应;
②溴与乙醛发生加成反应;
③由于醛基具有还原性,溴将乙醛氧化为乙酸.
为探究哪种猜想正确,小李同学提出了如下两种实验方案:
方案一:用pH试纸检测溴水褪色后溶液的酸碱性;
方案二:测定反应前溴水中Br2的物质的量和反应后溶液中Br-的物质的量.
(3)方案一是否可行否(填“是”或“否”),理由是 不论是发生取代反应还是发生氧化反应 溶液的酸性均增强.
(4)小李同学认为:假设测得反应前溴水中Br2的物质的量为amol,若测得反应后n(Br-)=amol,则说明溴与乙醛发生取代反应.
(5)小吴同学设计如下实验方案:
①按物质的量之比为1:5配制KBrO3-KBr溶液,加合适的适量的酸,完全反应并稀至1L,生成0.5molBr2.
②取上述溶液10mL加入足量乙醛溶液,使之褪色,然后将所得溶液稀释为100mL,准确量取其中10mL.
③加入过量的AgNO3溶液,过滤、洗涤、干燥后称量得到淡黄色固体0.188g.
试通过计算判断:溴与乙醛发生反应的化学方程式为CH3CHO+Br2+H2O→CH3COOH+2HBr.
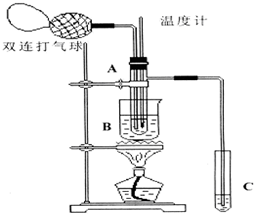
Ⅱ.小刘同学在查阅资料时得知,乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见下表:
| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$→_{CuO}^{60℃-80℃}$2CH3COOH.
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测量反应溶液的温度;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分.
(3)烧杯B内盛装的液体可以是乙二醇或甘油(写出一种即可,在题给物质中找).
| A. | 制取氧气时,用排水法收集氧气出现倒吸现象,立即打开试管上的橡皮塞 | |
| B. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| C. | 在气体发生装置上点燃氢气等气体时,必须先检验气体的纯度 | |
| D. | 给试管中的液体加热时,不停沿试管倾斜方向移动试管或加入碎瓷片,以免液体暴沸伤人 |
| A. | C3H8只表示一种物质的分子组成 | |
| B. | C2H6的一氯代物只有1种 | |
| C. | C3H8O能与钠反应放出H2的同分异构体有3种 | |
| D. | 丙烷的二氯代物有4种 |
| A. | $\frac{Vd}{MN+2240}$ | B. | $\frac{1000Vd}{MN-2240}$ | C. | $\frac{1000VdM}{MN+2240}$ | D. | $\frac{MN}{22.4(V+0.1)d}$ |
| A. | 氨水 | B. | 蔗糖 | C. | 干冰 | D. | 碳酸 |
| A. | 己烷有4种同分异构体,一定条件下能够发生取代反应 | |
| B. | 在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 | |
| C. | 油脂皂化反应属于取代反应 | |
| D. | 聚合物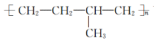 可由单体CH3CH═CH2和CH2═CH2加聚制得 可由单体CH3CH═CH2和CH2═CH2加聚制得 |
| A. | 乙烯的结构简式:CH2CH2 | B. | 甲烷的结构式CH4 | ||
| C. | 苯的分子式C6H6 | D. | 羟基:OH |
