题目内容
1.100mL6mol/LH2S04与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )| A. | 硫酸锌溶液 | B. | 氢氧化钠固体 | C. | 碳酸钠固体 | D. | 硫酸铜固体 |
分析 过量的锌粉反应,硫酸完全反应,为了减缓反应速率但又不影响生成氢气的总量,可减小氢离子浓度但不改变其物质的量,以此来解答.
解答 解:A.硫酸锌不与锌反应,但溶液体积增大,浓度减小,则反应速率减小,且又不影响生成氢气的总量,故A正确;
B.加入氢氧化钠,消耗硫酸,生成氢气的总量减少,故B错误;
C.加入碳酸钠,消耗硫酸,生成氢气的总量减少,故C错误;
D.锌置换出铜,形成原电池反应,加快反应速率,故D错误.
故选A.
点评 本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力的考查,注意信息中Zn过量及浓度对反应速率的影响即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
12.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 0.1mol•L-1Na2S溶液中含有0.2NA个Na+ | |
| B. | 标准状况下,22.4L的H2O含有2NA个氢原子 | |
| C. | 常温下,44gCO2含有NA个氧原子 | |
| D. | 0.1molNa与足量O2反应生成Na2O,转移0.1NA个电子 |
16.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如图:
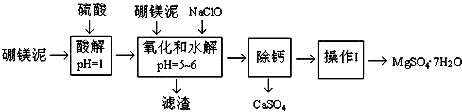
根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施升温、把硼镁泥粉碎、搅拌等.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+.
A.KSCN B.淀粉-KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤蒸发浓缩(结晶)、趁热过滤.
(6)现有l.60t硼镁泥,生产MgSO4•7H2O,若生产过程的产率为50%,则能生产出MgSO4•7H2O产品1.97t (计算结果保留三位有效数字).

根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施升温、把硼镁泥粉碎、搅拌等.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+.
A.KSCN B.淀粉-KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)现有l.60t硼镁泥,生产MgSO4•7H2O,若生产过程的产率为50%,则能生产出MgSO4•7H2O产品1.97t (计算结果保留三位有效数字).
6.下列有机物命名正确的是( )
| A. |  1,3,4-三甲苯 | B. |  2-甲基-2-氯丙烷 | C. |  2-甲基-1-丙醇 | D. |  2-甲基-3-丁炔 |
13.Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”.S2O32-和Cl2反应的产物之一为SO42-.下列说法中不正确的是( )
| A. | 该反应中Cl2发生还原反应 | |
| B. | 根据该反应可判断还原性:S2O32->Cl- | |
| C. | 脱氯反应后,溶液的酸性增强 | |
| D. | SO2与氯气的漂白原理相同,所以也可以用SO2作纺织工业的漂白剂 |
10.下列叙述正确的是( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 单质中一定存在共价键 | |
| C. | 共价化合物中一定存在共价键 | |
| D. | 离子化合物中只含有离子键 |
11.环保、安全的铝-空气电池的工作原理如图所示,下列有关叙述错误的是( )
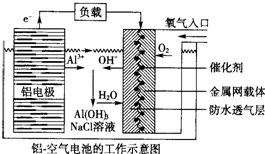

| A. | NaCl的作用是增强溶液的导电性 | |
| B. | 正极的电极反应式为O2+4e-+2H2O=4OH- | |
| C. | 电池工作过程中,电解质溶液的pH不断增大 | |
| D. | 用该电池作电源电解KI溶液制取1 mol KIO3,消耗铝电极的质量为54 g |
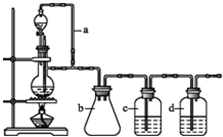 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
 ,该物质含有的化学键的类型是离子键、非极性共价键 .
,该物质含有的化学键的类型是离子键、非极性共价键 . .
.