题目内容
15. 实验室可用如图所示装置进行多个实验探究,请回答下列问题.
实验室可用如图所示装置进行多个实验探究,请回答下列问题.(1)若液体A为稀盐酸,试管中发生反应的化学方程式是Fe+2HCl=FeCl2+H2↑,反应现象是有气泡产生溶液变为浅绿色.
(2)若液体A为蒸馏水,放置一段时间后试管中的现象是在蒸馏水与空气的接触面附近,铁钉生锈严重.
(3)若一段时间后,观察到浸没在液体A中的铁钉表面覆盖一层红色物质,则试管中发生反应的化学方程式可能是Fe+CuSO4═Cu+FeSO4.
分析 (1)铁和盐酸反应能够生成氢气和氯化亚铁;
(2)铁发生电化学腐蚀;
(3)A中的铁钉表面覆盖一层红色物质,应为铜,铁置换出铜.
解答 解:(1)铁和盐酸反应能够生成氢气和氯化亚铁,方程式为Fe+2HCl=FeCl2+H2↑.氯化亚铁的溶液为浅绿色,故该反应的现象是有气泡产生溶液变为浅绿色,
故答案为:Fe+2HCl=FeCl2+H2↑;有气泡产生溶液变为浅绿色;
(2)若液体A为蒸馏水则铁钉具备与氧气和水共存的条件,所以会发现铁钉在水外面的部分会生锈,故答案为:在蒸馏水与空气的接触面附近,铁钉生锈严重;
(3)若一段时间后,观察到浸没在A中的铁钉表面覆盖一层红色物质,则是铁和硫酸铜溶液发生置换反应的过程,方程式为Fe+CuSO4═Cu+FeSO4;
故答案为:Fe+CuSO4═Cu+FeSO4.
点评 本题综合考查铁的性质,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意铁发生电化学腐蚀的条件,难度不大.

练习册系列答案
相关题目
6.下列分子中所有原子未全部满足最外层为8个电子结构的是( )
| A. | N2 | B. | CO2 | C. | BF3 | D. | PCl3 |
3.据报道,化学家创造出对CO2有较强吸收能力的粉末状物质--“干水”,其每个颗粒的外层是SiO2,内部含水95%.下列有关说法正确的是( )
| A. | 干水属于有机合成材料 | |
| B. | 干水中的水分子停止运动 | |
| C. | 干水是一种混合物 | |
| D. | 干水吸收CO2的过程只发生物理变化 |
7.下列是A、B、C、D、E五种元素的某些性质:
(1)元素A是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是D.
A.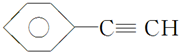 B.CH4
B.CH4
C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
| A | B | C | D | E | |
| 化合价 | -4 | -2 | -1 | -2 | -1 |
| 电负性 | 2.55 | 2.58 | 3.16 | 3.44 | 3.98 |
A.
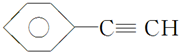 B.CH4
B.CH4C.CH2═CHCH3 D.CH3CH2C≡CH E.CH3CH3
(2)用氢键表示式写出E的氢化物的水溶液中存在的所有氢键F-H…F、F-H…O、O-H…F、O-H…O.
(3)相同条件下,AD2与BD2分子在水中的溶解度较大的是SO2(化学式),理由是因为CO2是非极性分子,SO2和H2O都是极性分子,根据“相似相溶”原理,SO2在H2O中的溶解度较大.
(4)B、D形成的氢化物沸点:H2O更高,热稳定性H2O更强.(写化学式)
5.任何科学真理的发现,都不是一帆风顺的,门捷列夫的元素周期表奠定了现代化学和物理学的理论基础.下列关于元素周期表的说法中,不正确的是( )
| A. | 周期表中的副族、Ⅷ族都是金属元素 | |
| B. | 周期表中的ⅡA族都是金属元素 | |
| C. | 周期表中的非金属元素都位于短周期 | |
| D. | 周期表中的0族元素都是非金属元素 |
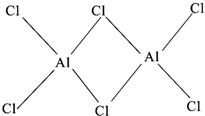 有机反应中常用镍作催化剂.某镍催化剂中含Ni 64.0%、Al 24.3%、Fe 1.4%,其余为C、H、O、N等元素.
有机反应中常用镍作催化剂.某镍催化剂中含Ni 64.0%、Al 24.3%、Fe 1.4%,其余为C、H、O、N等元素.
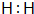 .
.