题目内容
7.下列各项有机化合物的分类方法及所含官能团都正确的是( )| A. | 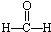 醛类 醛类 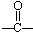 | B. | 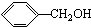 酚类-OH 酚类-OH | C. | 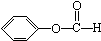 醛类 醛类 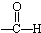 | D. | CH3COOH 羧酸类 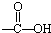 |
分析 A.醛的官能团为-CHO;
B.-OH与苯环直接相连的为酚;
C.含-COOC-;
D.含-COOH.
解答 解:A.醛的官能团为-CHO,则HCHO为醛类物质,故A不选;
B.-OH与苯环直接相连的为酚,则 为醇类,故B不选;
为醇类,故B不选;
C.含-COOC-,则 为酯类物质,故C不选;
为酯类物质,故C不选;
D.含-COOH,则CH3COOH为羧酸,故D选;
故选D.
点评 本题考查有机物的官能团及分类,为高考常见题型,侧重于学生的分析能力的考查,注意把握常见有机物的官能团为解答该类题目的关键,题目难度不大.

练习册系列答案
相关题目
18.恒温下,在容积为2L的恒容密闭容器中发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0,n(SO2)随时间变化关系如表:
下列说法正确的是( )
| 时间/m i n | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.2 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A. | 当容器中气体的密度不变时,该反应达到平衡状态 | |
| B. | 用SO3表示0~4 min内该反应的平均速率为0.01 mol/(L•m i n) | |
| C. | 升高温度时,逆反应速率大于正反应速率,平衡常数K值会减小 | |
| D. | 平衡时再通入18O2,平衡右移,达新平衡时,18O仅存在于O2和SO3中 |
15.在水电离出的c(H+)=1×10-14 mol•L-1的溶液中,一定能大量共存的离子组是( )
| A. | K+、Na+、HCO3-、Cl- | B. | K+、AlO2-、Br-、Cl- | ||
| C. | Na+、Cl-、NO3-、SO42- | D. | Al3+、NH4+、Cl-、SO42- |
2.设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 常温常压下,11.2 LCO2所含的原子数为1.5NA | |
| B. | 标准状况下,22.4 L CCl4中所含分子数为NA | |
| C. | 标准状况下,18g水所含原子数为NA | |
| D. | 常温常压下,48 g O2与O3混合物含有的氧原子数为3NA |
12.回答下列问题.
(1)浓硫酸与木炭在加热条件下反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+SO2+2H2O
(2)试用如图所列各种装置设计一个实验来验证上述反应所产生的各种产物
这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):4→2→1→3.
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物中是否有二氧化硫,B瓶溶液的作用是除去二氧化硫,C瓶溶液的作用是确定产物中二氧化硫已经被B瓶溶液除尽.
(4)装置②中所加固体药品是无水硫酸铜,可验证的产物是H2O,确定装置②在整套装置中位置的理由是由于产物气流通过装置1、3带出水蒸气,所以2必须在1、3之前.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是二氧化碳.
(1)浓硫酸与木炭在加热条件下反应的化学方程式是C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+SO2+2H2O
(2)试用如图所列各种装置设计一个实验来验证上述反应所产生的各种产物
| 编号 | ① | ② | ③ | ④ |
| 装置 | 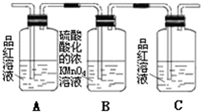 | 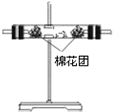 | 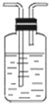 | 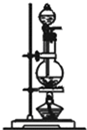 |
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是验证产物中是否有二氧化硫,B瓶溶液的作用是除去二氧化硫,C瓶溶液的作用是确定产物中二氧化硫已经被B瓶溶液除尽.
(4)装置②中所加固体药品是无水硫酸铜,可验证的产物是H2O,确定装置②在整套装置中位置的理由是由于产物气流通过装置1、3带出水蒸气,所以2必须在1、3之前.
(5)装置③中所盛溶液是澄清石灰水,可验证的产物是二氧化碳.
16.下列说法正确的是( )
| A. | 原子最外层电子数等于或大于4的元素一定是非金属元素 | |
| B. | 原子最外层只有2个电子的元素一定是金属元素 | |
| C. | 最外层电子数比次外层电子数多的元素一定位于第二周期 | |
| D. | 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期 |
17.表是元素周期表的一部分,回答下列问题:
(1)写出①、②两种元素的名称:碳、氮.
(2)写出⑧、⑨两种元素的符号:Si、P.
(3)在这些元素中,最活泼的金属的离子结构示意图是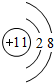 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
| 族 周期 | IA | IIA | IIIA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)写出⑧、⑨两种元素的符号:Si、P.
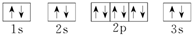
(3)在这些元素中,最活泼的金属的离子结构示意图是
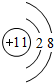 ,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.
,最活泼的非金属元素是F (填元素符号,下同),Ar是最不活泼的元素.(4)这些元素的最高价氧化物对应水化物中,HClO4(填化学式,下同)酸性最强,NaOH的碱性最强;能形成两性氢氧化物的元素是Al(填元素符号).
(5)在⑤到⑪的元素中,Cl(填元素符号)原子半径最小.
(6)比较⑤和⑥的化学性质,Na(填元素符号)更活泼,试用实验证明之(简述操作、现象和结论)金属钠与金属镁单质分别与冷水反应,反应剧烈程度大的是钠,反之是镁.
 ;D
;D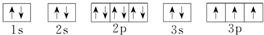 .
.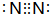 ,氢化物
,氢化物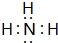 .
.