题目内容
14.化学学科需要借助化学专用语言描述,下列有关化学用语正确的是( )| A. | CO2分子比例模型: | B. | NH4I的电子式: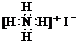 | ||
| C. | 乙醇的结构简式:C2H5OH | D. | K+最外层电子排布式:4S24P6 |
分析 A.比例模型中用不同体积的小球表示不同原子的大小,碳的原子半径比氧的大;
B.碘离子用括号,应标出电子;
C.结构简式是把结构式中的单键省略之后的一种简略表达形式;
D.K原子失去一个电子得到钾离子.
解答 解:A.碳和氧位于同一周期,从左到右原子半径逐渐减小,故碳的原子半径较大,CO2分子比例模型: ,故A错误;
,故A错误;
B.NH4I的电子式为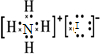 ,故B错误;
,故B错误;
C.乙醇的结构简式:C2H5OH,故C正确;
D.K+最外层电子排布式:3S23P6,故D错误.
故选C.
点评 本题考查常用的化学用语,难度不大,学生应注意利用原子的结构来分析电子式及原子之间的成键,并注意化学用语书写的规范性来解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.阿伏伽德罗常数约为6.02×1023mol-1.下列叙述中正确的是( )
| A. | 标准状况下,4.48LCH3CH2OH中约含有1.204×1023个羟基 | |
| B. | 常温常压下,31g白磷P4和红磷P8的混合中约含有6.02×1023个磷原子 | |
| C. | 标准状况下,7.8g苯中约含有1.806×1023个碳碳双键 | |
| D. | 1molH2O2在MnO2催化作用下完全反应转移的电子数约为1.204×1024个电子 |
9.金丝桃素的结构简式如图所示,下列有关它的说法正确的是( )


| A. | 属于芳香烃 | B. | 分子中苯环上的一氯代物有3种 | ||
| C. | 不能与金属钠发生反应 | D. | 不能发生水解反应 |
19.下列离子方程式中正确的是( )
| A. | 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-→CuS↓+H2S↑ | |
| B. | Fe3O4溶解在过量的稀硝酸中:Fe3O4+8H+→Fe2++2Fe3++4H2O | |
| C. | 碳酸氢铵溶液与苛性钾溶液混和共热:NH4++OH-→NH3↑+H2O | |
| D. | 将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
6.下列表示物质结构的化学用语正确的是( )
| A. | CH4分子的比例模型: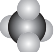 | B. | CO2的电子式:O::C::O | ||
| C. | Cl-的离子结构示意图: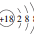 | D. | 中子数为18的硫原子:${\;}_{16}^{18}$S |
3.室温下,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1mol•L-1的CH3COOH溶液中:c(CH3COO-)>c(H+)>c(OH-) | |
| B. | 0.1mol•L-1的NaHCO3溶液中:c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 0.1mol•L-1的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| D. | 0.1mol•L-1的NH4Cl溶液中:c(NH4+)+c(H+)=c(NH3•H2O)+c(OH-) |
4.NA为阿伏伽德罗常数的竖直,下列说法中正确的是( )
| A. | 在密闭容器中加入15mol H2和0.5mol N2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3g的Na完全与O2反应时失去的电子数为0.1NA | |
| C. | 0.1L的0.1mol•L-1 Na2S溶液中含有的S2-离子数为0.1NA | |
| D. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |