题目内容
研究发现,空气中少量的NO2能作为催化剂参与硫酸型酸雨的形成,NO2在上述过程中的作用,与H2SO4在下述变化中的作用相似的是( )
| A、硫化氢通入浓H2SO4中 |
| B、稀H2SO4和乙酸乙酯共热 |
| C、浓H2SO4和C2H5OH共热到170℃ |
| D、潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
考点:浓硫酸的性质,氯气的化学性质,硫化氢
专题:元素及其化合物
分析:空气中少量的NO2能作为催化剂参与硫酸型酸雨的形成,说明该反应中二氧化氮作催化剂,起催化作用,据此分析解答.
解答:
解:空气中少量的NO2能作为催化剂参与硫酸型酸雨的形成,说明该反应中二氧化氮作催化剂,起催化作用,
A.硫化氢通入浓H2SO4中,二者反应生成S和二氧化硫,浓硫酸得电子作氧化剂,体现氧化性,故A错误;
B.乙酸乙酯和稀硫酸共热,稀硫酸作催化剂促进乙酸乙酯水解,起催化作用,故B正确;
C.浓硫酸和C2H5OH共热到170℃,浓硫酸体现催化性和脱水性,故C错误;
D.潮湿的氯气通过盛有浓H2SO4的洗气瓶,浓硫酸吸收水分而导致氯气干燥,浓硫酸体现吸水性,故D错误;
故选B.
A.硫化氢通入浓H2SO4中,二者反应生成S和二氧化硫,浓硫酸得电子作氧化剂,体现氧化性,故A错误;
B.乙酸乙酯和稀硫酸共热,稀硫酸作催化剂促进乙酸乙酯水解,起催化作用,故B正确;
C.浓硫酸和C2H5OH共热到170℃,浓硫酸体现催化性和脱水性,故C错误;
D.潮湿的氯气通过盛有浓H2SO4的洗气瓶,浓硫酸吸收水分而导致氯气干燥,浓硫酸体现吸水性,故D错误;
故选B.
点评:本题考查硫酸的性质,明确浓硫酸具有吸水性、脱水性、强氧化性和酸性,注意吸水性和脱水性的区别,题目难度不大.

练习册系列答案
相关题目
在有机物分子中,若某个碳原子连接着四个不同的原子或原子团,这种碳原子称为手性碳原子,凡是有一个手性碳原子的物质一定具有光学活性.例如,有机化合物 有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
 有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )
有光学活性,分别发生下列反应:①与甲酸发生酯化反应②与氢氧化钠水溶液共热③与银氨溶液作用④在催化剂存在下与氢气作用.生成的有机物中无光学活性的是( )| A、①②④ | B、②③④ |
| C、①②③ | D、①③④ |
向一定量的盐酸中逐滴加入NaAlO2溶液,生成沉淀Al(OH)3的量随NaAlO2加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )

A、a点对应的溶液中:NH
| ||||||
B、b点对应的溶液中:Na+、S2-、SO
| ||||||
C、c点对应的溶液中:Ag+、Ba2+、K+、NO
| ||||||
D、d点对应的溶液中:K+、S2-、I-、CO
|
下列叙述正确的是( )
| A、25℃时,0.1mol/L的醋酸中,c(H+)=0.1mol/L | ||
| B、在稀醋酸溶液中加入少量醋酸钠固体,会促进醋酸的电离 | ||
| C、在稀氨水中通入氨气,所得溶液的pH减小 | ||
D、向0.1mol/L的氨水中加入少量硫酸铵固体,则溶液中
|
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、0.1mol?L-1的NH4Cl溶液C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| B、0.1mol?L-1的(NH4)2SO4溶液中:C(NH4+)=2 C(SO42-) |
| C、0.2mol?L-1的Na2CO3溶液中:C(OH-)=C(HCO3-)+C(H+)+C(H2CO3) |
| D、C(NH4+)相等的NH4HSO4溶液,NH4HCO3溶液和NH4Cl溶液中,C(NH4H SO4)<C( NH4Cl)<C(NH4HCO3) |
2011年3月11日,日本本州岛仙台港发生9.0级地震,地震引发海啸、食盐、蔗糖、醋酸、“84消毒液”、明矾等是灾后居民日常生活中经常使用的物质,下列有关说法或表示正确的是( )
A、食盐中阴离子的结构示意图为: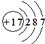 |
| B、蔗糖和醋酸都是弱电解质 |
C、“84消毒液”中有效成分NaClO的电子式为: |
| D、明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |