题目内容
配制100mL 0.1mol?L-1 Na2CO3溶液,下列操作正确的是( )
| A、称取1.06 g 无水碳酸钠,加入100 mL 容量瓶中,加水溶解、定容 |
| B、称取1.06 g 无水碳酸钠,加入蒸馏水,搅拌、溶解,配制100 mL溶液 |
| C、转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中 |
| D、定容后,塞好瓶塞,反复倒转,摇匀 |
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:A、容量瓶不能作为溶解仪器;
B、根据n=CV和m=nM来计算出需要Na2CO3的质量,最后使溶液的体积是100ml;
C、移液操作需要玻璃棒来引流;
D、根据配制溶液的实验步骤来回答.
B、根据n=CV和m=nM来计算出需要Na2CO3的质量,最后使溶液的体积是100ml;
C、移液操作需要玻璃棒来引流;
D、根据配制溶液的实验步骤来回答.
解答:
解:A、容量瓶不能作为溶解仪器,称量固体后不能在容量瓶中溶解,应先在烧杯中溶解,故A错误;
B、根据n=CV可知Na2CO3的物质的量n=0.1L×0.1mol?L-1=0.01mol,质量m=nM=0.01mol×106g/mol=1.06g,取1.06 g 无水碳酸钠,加入蒸馏水,搅拌、溶解,配制成100 mL溶液即可,故B正确;
C、移液操作时,防止液体外溅,需要玻璃棒来引流,故C错误;
D、定容后,塞好瓶塞,要进行摇匀操作,故D正确.
故选BD.
B、根据n=CV可知Na2CO3的物质的量n=0.1L×0.1mol?L-1=0.01mol,质量m=nM=0.01mol×106g/mol=1.06g,取1.06 g 无水碳酸钠,加入蒸馏水,搅拌、溶解,配制成100 mL溶液即可,故B正确;
C、移液操作时,防止液体外溅,需要玻璃棒来引流,故C错误;
D、定容后,塞好瓶塞,要进行摇匀操作,故D正确.
故选BD.
点评:本题是一道关于配制一定物质的量浓度溶液的实验基本操作题,可以根据教材知识来回答,难度不大.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
下列有关试剂的保存方法,错误的是( )
| A、铝片直接放置在空气中 |
| B、漂白粉保存在烧杯中 |
| C、新制的氯水通常保存在棕色细口玻璃试剂瓶中 |
| D、氢氧化钠溶液用带橡胶塞的试剂瓶贮存 |
两种气态烃组成的混合物共0.1mol,完全燃烧后得到4.48LCO2(标准状况下)和3.6g水,则这两种气体可能是( )
| A、CH4和C3H8 |
| B、CH4和C3H4 |
| C、C2H4和C3H4 |
| D、C2H4和C2H6 |
下列离子方程式正确的是( )
| A、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2→2 Fe3++2H2O |
| D、向NaHCO3 溶液中加入过量Ca(OH)2 溶液:2HCO3-+Ca2++2OH-→2H2O+CaCO3↓+CO32- |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B、标准状况下,以任意比混合的氢气和一氧化碳气体共8.96L,在足量氧气中充分燃烧时消耗氧气的分子数为0.2NA |
| C、含1 mol FeCl3的溶液中Fe3+的个数为NA |
| D、1.8 g NH4+中含有的电子数为0.1NA |
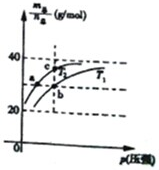 已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )| A、平衡常数K(a)=K(b)<K(c) | ||
| B、反应速率:va<vb | ||
| C、温度:T2>T1 | ||
D、当
|
从宏观上来说物质由元素组成,从微观上物质由粒子构成,下列说法不正确的是( )
| A、54Fe和56Fe互为同位素 |
| B、质子数等于电子数的某微粒,可能是一种分子或离子 |
| C、只有一种分子组成的一定为纯净物 |
| D、16gO2和16gO3含有的原子数相等 |
除去NaCl溶液中MgC12、CaC12的方法是( )
| A、将样品溶于蒸馏水,加入过量NaOH过滤后,加盐酸蒸发 |
| B、将样品溶于蒸馏水,加入过量 Na2CO3过滤后,加盐酸蒸发 |
| C、将样品溶于蒸馏水,加入过量Ca(OH)2过滤,然后加过量Na2CO3过滤,在滤液中加过量盐酸后蒸发 |
| D、用半透膜有选择地除去Ca2+、Mg2+ |
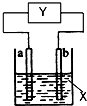 如图装置中a为纯铜棒,Y为电路的未知部分,X为某种液体,下列说法正确的是( )
如图装置中a为纯铜棒,Y为电路的未知部分,X为某种液体,下列说法正确的是( )