题目内容
下列离子方程式正确的是( )
| A、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-→BaSO4↓+H2O |
| B、将少量SO2气体通入NaClO溶液中:SO2+2ClO-+H2O→SO32-+2HClO |
| C、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:2Fe2++2H++H2O2→2 Fe3++2H2O |
| D、向NaHCO3 溶液中加入过量Ca(OH)2 溶液:2HCO3-+Ca2++2OH-→2H2O+CaCO3↓+CO32- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.溶液显示中性,则硫酸氢钾与氢氧化钡按照物质的量2:1反应,离子方程式按照氢氧化钡的组成书写;
B.次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子,反应产物应该为硫酸根离子;
C.亚铁离子被双氧水氧化成铁离子,根据电荷守恒、电子守恒进行判断;
D.氢氧化钙过量,反应产物中不会剩余碳酸根离子,离子方程式按照碳酸氢钠的组成书写.
B.次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子,反应产物应该为硫酸根离子;
C.亚铁离子被双氧水氧化成铁离子,根据电荷守恒、电子守恒进行判断;
D.氢氧化钙过量,反应产物中不会剩余碳酸根离子,离子方程式按照碳酸氢钠的组成书写.
解答:
解:A.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7,硫酸氢钾与氢氧化钡的物质的量之比为2:1,反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故A错误;
B.将少量SO2气体通入NaClO溶液中,二氧化硫被氧化成硫酸根离子,正确的离子方程式为:ClO-+H2O+SO2═SO42-+2H++Cl-,故B错误;
C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液,亚铁离子被氧化成铁离子,反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,故C正确;
D.向NaHCO3 溶液中加入过量Ca(OH)2 溶液,氢氧化钙过量,离子方程式按照碳酸氢钠的组成书写,碳酸氢钠完全转化成碳酸钙沉淀,正确的离子方程式为:HCO3-+Ca2++OH-=H2O+CaCO3↓,故D错误;
故选C.
B.将少量SO2气体通入NaClO溶液中,二氧化硫被氧化成硫酸根离子,正确的离子方程式为:ClO-+H2O+SO2═SO42-+2H++Cl-,故B错误;
C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液,亚铁离子被氧化成铁离子,反应的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O,故C正确;
D.向NaHCO3 溶液中加入过量Ca(OH)2 溶液,氢氧化钙过量,离子方程式按照碳酸氢钠的组成书写,碳酸氢钠完全转化成碳酸钙沉淀,正确的离子方程式为:HCO3-+Ca2++OH-=H2O+CaCO3↓,故D错误;
故选C.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等;选项B为易错点,注意次氯酸具有强氧化性.

练习册系列答案
相关题目
如列图象及对应说法正确的是( )


| A、图1表示恒温恒压下条件,向2HI?H2+I2△H>0的反应达到平衡的容器中充入HI,甲表示正反应速率,乙表示逆反应速率 |
| B、图1表示恒容下条件,向2HI?H2+I2△H>0的反应达到平衡的容器加热,甲表示正反应速率,乙表示逆反应速率 |
| C、图2表示恒温条件下,压缩2SO3(g)?2SO2(g)+O2(g)△H>0平衡反应体系,甲表示的SO3物质的量的变化,乙表示的SO3物质的量浓度的变化 |
| D、图2表示恒容条件下,对于2SO3(g)?2SO2(g)+O2(g)△H>0反应平衡体系,甲表示升高温度SO3物质的量的变化,乙表示增加O2后SO3物质的量变化 |
将Na2O2逐渐加入到含有H+、Mg2+、Al3+、NH4+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入的Na2O2物质的量(mol)的关系如图所示,则原溶液中的Mg2+、Al3+、NH4+物质的量分别( )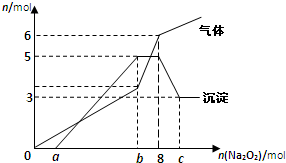

| A、2 mol、3 mol、6 mol |
| B、3 mol、2 mol、6mol |
| C、2 mol、3 mol、4 mol |
| D、3 mol、2 mol、2 mol |
根据下列物质的性质,判断其应用错误的是( )
| A、碳酸钠溶液呈碱性,可用于清洗油污 |
| B、水与乙醇以任意比例互溶,可用水洗、分液的方法除去溴乙烷中的乙醇 |
| C、镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
| D、游泳池中常加入硫酸铜,其主要作用是铜离子水解生成Cu(OH)2胶体,能吸咐池中的悬浮物 |
下列依据热化学方程式得出的结论正确的是( )
| A、已知2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ?mol-1说明2mol H2(g)和1mol O2(g)的能量总和小于2molH2O(g)的能量 |
| B、已知C(s,石墨)═C(s,金刚石)△H>0,则金刚石比石墨稳定 |
| C、已知2C(s)+2O2(g)═2CO2(g)△H1 2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
| D、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ?mol-1,则含20gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的热量 |
配制100mL 0.1mol?L-1 Na2CO3溶液,下列操作正确的是( )
| A、称取1.06 g 无水碳酸钠,加入100 mL 容量瓶中,加水溶解、定容 |
| B、称取1.06 g 无水碳酸钠,加入蒸馏水,搅拌、溶解,配制100 mL溶液 |
| C、转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中 |
| D、定容后,塞好瓶塞,反复倒转,摇匀 |
下列有关碳酸钠和碳酸氢钠的叙述中正确的是( )
| A、等质量的两种盐分别与足量盐酸反应,碳酸钠产生的气体多 |
| B、等质量的两种盐分别与足量盐酸反应,碳酸钠反应更剧烈 |
| C、盐酸滴加到碳酸钠溶液中与碳酸钠溶液滴加到盐酸中,两者的现象相同 |
| D、盐酸滴加到碳酸氢钠溶液中与碳酸氢钠溶液滴加到盐酸中,两者的现象相同 |
下列说法正确的是( )
| A、人体缺少维生素A易患夜盲症、干眼症 |
| B、玻璃钢广泛用于制造汽车车身、船体和印刷电路板 |
| C、为使火腿肠颜色更鲜红,可多加一些亚硝酸钠 |
| D、碳酸氢钠可作抗酸药,阿司匹林是重要的抗生素 |
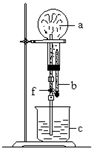 在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )
在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )