题目内容
在一定条件下,对于密闭容器中进行的反应:P(g)+Q(g)?R(g)+S(g),下列说法可以充分说明这一反应达到平衡状态的是( )
| A、容器内的压强不再变化 |
| B、各物质的浓度相等 |
| C、P、Q、R、S共存 |
| D、用Q表示的正反应速率与用S表示的逆反应速率相等 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量不变,注意该反应中气体的化学计量数之和前后相等的特点.
解答:
解:A.从反应开始到平衡容器内的压强一直不变化,故A错误;
B.各物质的浓度相等,并不是不变,故B错误;
C.反应物和生成物共存这是可逆反应的特征,故C错误;
D.反应速率之比等于化学计量数之比,用S的浓度表示的化学反应速率与用Q的浓度表示的化学反应正逆反应速率相等,能说明正逆反应速率相等,故D正确.
故选D.
B.各物质的浓度相等,并不是不变,故B错误;
C.反应物和生成物共存这是可逆反应的特征,故C错误;
D.反应速率之比等于化学计量数之比,用S的浓度表示的化学反应速率与用Q的浓度表示的化学反应正逆反应速率相等,能说明正逆反应速率相等,故D正确.
故选D.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
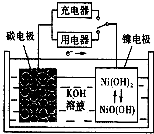 用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A、放电时,负极的电极反应为:H2-2e-+2OH-=2H2O |
| B、充电时,阳极的电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O |
| C、放电时,OH-移向镍电极 |
| D、充电时,将电池的碳电极与外电源的正极相连 |
用NA表示阿伏加德罗常数的值.下列说法一定正确的是( )
| A、1 mol苯乙烯中含碳碳双键数为4NA |
| B、30 g 甲醛和醋酸的混合物中含碳原子数目为NA |
| C、标准状况下,22.4 L空气含单质分子数目为NA |
| D、0.5 mol Na2O2溶解于1 L水中得Na+的物质的量浓度为1 mol?L-1 |
一定量的锌粉和2mol?L-1的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2总量的是( )
①石墨;②CuO;③铜粉;④KNO3;⑤浓盐酸;⑥无水硫酸铜.
①石墨;②CuO;③铜粉;④KNO3;⑤浓盐酸;⑥无水硫酸铜.
| A、①③④ | B、①③⑤ |
| C、②④⑥ | D、②⑤⑥ |
下列物质均能与水发生反应形成新的物质.下列化学方程式中正确的是( )
①ICl+H2O═HI+HClO
②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl
④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
①ICl+H2O═HI+HClO
②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl
④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
| A、①④ | B、②③ |
| C、①②④ | D、②③④ |
下列化学用语正确的是( )
| A、乙烯的结构简式 C2H4 |
B、苯分子的结构式 |
C、氯离子的结构示意图  |
D、水的电子式 |
下列关于有机物的说法正确的是( )
| A、油脂在人体内水解为氨基酸和甘油等小分子后被人体吸收 |
| B、甲酸甲酯(HCOOCH3)和乙酸是同分异构体 |
| C、石油催化裂化的主要目的是提高芳香烃的产量 |
D、聚丙烯的结构简式为 |
下列说法正确的是( )
| A、蛋白质的变性是一个可逆过程 |
| B、蔗糖和麦芽糖的水解产物完全相同 |
| C、误服重金属盐,立即服用牛奶或豆浆可解毒 |
| D、糖类、脂类、蛋白质都属于天然高分子化合物 |
 铝和氢氧化钾都是重要的工业产品.请回答:
铝和氢氧化钾都是重要的工业产品.请回答: