题目内容
下列物质均能与水发生反应形成新的物质.下列化学方程式中正确的是( )
①ICl+H2O═HI+HClO
②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl
④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
①ICl+H2O═HI+HClO
②CH3COCl+H2O→CH3COOH+HCl
③SiCl4+4H2O═H4SiO4+4HCl
④Mg3N2+6H2O═3Mg(OH)2+2NH3↑
| A、①④ | B、②③ |
| C、①②④ | D、②③④ |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:反应时各物质和水均分别离解成两部分,然后再两两重新组合,形成新的物质,注意根据化合价的正负组合.
解答:
解:①ICl中碘的化合价为+1价,氯的化合价为-1价,则ICl+H2O═HIO+HCl,故错误;
②CH3COCl中氯的化合价为-1价,则CH3COCl+H2O=CH3COOH+HCl,故正确;
③SiCl4中氯的化合价为-1价,则SiCl4+4H2O═H4SiO4+4HCl,故正确;
④Mg3N2中氮的化合价为-3价,则Mg3N2+6H2O═3Mg(OH)2+2NH3↑,故正确;
故选:D;
②CH3COCl中氯的化合价为-1价,则CH3COCl+H2O=CH3COOH+HCl,故正确;
③SiCl4中氯的化合价为-1价,则SiCl4+4H2O═H4SiO4+4HCl,故正确;
④Mg3N2中氮的化合价为-3价,则Mg3N2+6H2O═3Mg(OH)2+2NH3↑,故正确;
故选:D;
点评:本题培养了学生分析问题的能力,难度中等,注意根据化合价的正负组合.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
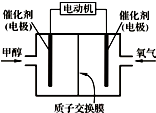 甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )
甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )| A、外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B、通甲醇一端为负极 |
| C、正极反应为:O2+4H++4e-=2H2O |
| D、负极反应为:CH3OH+H2O+6e-=CO2↑+6H+ |
电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4、H2YO4、H3ZO4,则下列判断错误的是( )
| A、原子半径X>Y>Z |
| B、气态氢化物的稳定性HX>H2Y>ZH3 |
| C、非金属性X>Y>Z |
| D、气态氢化物的还原性HX<H2Y<ZH3 |
在一定条件下,对于密闭容器中进行的反应:P(g)+Q(g)?R(g)+S(g),下列说法可以充分说明这一反应达到平衡状态的是( )
| A、容器内的压强不再变化 |
| B、各物质的浓度相等 |
| C、P、Q、R、S共存 |
| D、用Q表示的正反应速率与用S表示的逆反应速率相等 |
 化合物M叫假蜜环菌甲素(如图),它是香豆素类天然化合物.对M性质叙述正确的是( )
化合物M叫假蜜环菌甲素(如图),它是香豆素类天然化合物.对M性质叙述正确的是( )| A、M能与FeCl3发生反应,不能与CH3COOH发生反应 |
| B、M与Br2只能发生取代反应,不能发生加成反应 |
| C、1molM最多可消耗3mol NaOH |
| D、1molM在催化剂作用下最多能与4molH2发生加成反应 |
下列离子方程式中正确的是( )
| A、某钾盐K2A 的水溶液显碱性,其原因是:A2-+2H2O?H2A+2OH- | ||||||
| B、在30mL 1mol?L-1的Na2SO3溶液中通入标准状况下的Cl2 224mL:H2O+3SO32-+Cl2═SO42-+2HSO3-+2Cl- | ||||||
C、碳酸氢铵溶液与足量的NaOH溶液混合加热:NH
| ||||||
D、在Ba(HCO3)2溶液中逐滴滴入NaHSO4 溶液至Ba2+恰好完全沉淀时:Ba2++2HCO
|
下列关于溶液和胶体的叙述,正确的是( )
| A、一束光线分别通过溶液和胶体时,后者能看到一条光亮的“通路”,前者则没有 |
| B、溶液是电中性的,胶体是带电的 |
| C、溶液中溶质分子可以通过滤纸,胶体中分散质粒子则不能通过滤纸 |
| D、通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动 |
 常温下,向10mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、pH=7时,所加醋酸溶液的体积为10mL |
| B、pH<7时,溶液中c(CH3COO-)>c(Na+) |
| C、7<pH<13时,溶液中c(Na+)+c(H+)>c(CH3COOH)+c(OH-) |
| D、继续滴加0.1 mol?L-1醋酸溶液,溶液pH可以变为1 |