题目内容
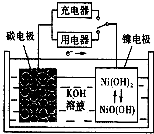 用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A、放电时,负极的电极反应为:H2-2e-+2OH-=2H2O |
| B、充电时,阳极的电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O |
| C、放电时,OH-移向镍电极 |
| D、充电时,将电池的碳电极与外电源的正极相连 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、放电时,负极上氢气失电子发生氧化反应;
B、充电时,阳极上发生失电子的氧化反应;
C、放电时,电解质溶液中阴离子向负极移动;
D、该电池充电时,碳电极与电源的负极相连.
B、充电时,阳极上发生失电子的氧化反应;
C、放电时,电解质溶液中阴离子向负极移动;
D、该电池充电时,碳电极与电源的负极相连.
解答:
解:A、放电时,负极上氢气失电子发生氧化反应,电极反应式为H2+2OH--2e-═2H2O,故A正确;
B、放电时,阳极上发生失电子的氧化反应,即Ni(OH)2+OH--e-=NiO(OH)+H2O,故B正确;
C、放电时,该电池为原电池,电解质溶液中阴离子向负极移动,所以OH-移向碳电极,故C错误;
D.该电池充电时,碳电极附近物质要恢复原状,则应该得电子发生还原反应,所以碳电极作阴极,应该与电源的负极相连,故D错误;
故选:AB.
B、放电时,阳极上发生失电子的氧化反应,即Ni(OH)2+OH--e-=NiO(OH)+H2O,故B正确;
C、放电时,该电池为原电池,电解质溶液中阴离子向负极移动,所以OH-移向碳电极,故C错误;
D.该电池充电时,碳电极附近物质要恢复原状,则应该得电子发生还原反应,所以碳电极作阴极,应该与电源的负极相连,故D错误;
故选:AB.
点评:本题考查了原电池和电解池原理,明确正负极上发生的电极反应及阴阳离子的移动方向即可解答,易错选项是D,注意结合电解原理确定与原电池哪个电极相连,为易错点.

练习册系列答案
相关题目
关于Ca元素和Cl元素的叙述正确的是( )
| A、原子序数Ca>Cl |
| B、原子半径Ca<Cl |
| C、原子的电子层数Ca<Cl |
| D、原子最外层电子数Ca>Cl |
下列说法错误的是( )
| A、食醋用氢氧化钠溶液滴定开始时,溶液的PH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃 |
| B、纸层析法分离铁离子和铜离子实验中,点样后的滤纸晾干后将其末端浸入展开剂中约0.5cm |
| C、Cu2+与足量氨水反应的离子方程式 Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
| D、硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 |
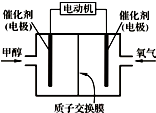 甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )
甲醇(CH3OH)燃料电池可用作电动汽车电源,如图为电池示意图.在电池的一极通入甲醇,另一极通入氧气,工作时H+由负极移向正极.下列叙述不正确的是( )| A、外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
| B、通甲醇一端为负极 |
| C、正极反应为:O2+4H++4e-=2H2O |
| D、负极反应为:CH3OH+H2O+6e-=CO2↑+6H+ |
北京奥运会“祥云”火炬所用燃料为丙烷,下列有关丙烷叙述中不正确的是( )
| A、比二氯甲烷的沸点高 |
| B、与甲烷互为同系物 |
| C、分子中的碳原子一定在同一平面上 |
| D、丙烷没有同分异构体 |
在一定条件下,对于密闭容器中进行的反应:P(g)+Q(g)?R(g)+S(g),下列说法可以充分说明这一反应达到平衡状态的是( )
| A、容器内的压强不再变化 |
| B、各物质的浓度相等 |
| C、P、Q、R、S共存 |
| D、用Q表示的正反应速率与用S表示的逆反应速率相等 |
下列溶液中的氯离子浓度与50mL0.1mol/L氯化铝溶液中的氯离子浓度相等的是( )
| A、150mL 0.1mol/L NaCl |
| B、75mL 0.2mol/L NH4Cl |
| C、100mL 0.3mol/L KCl |
| D、150mL 0.1mol/L FeCl3 |
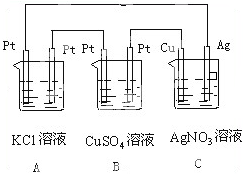 如图所示,若反应一段时间,5min时铜电极质量增加1.08g,试回答:
如图所示,若反应一段时间,5min时铜电极质量增加1.08g,试回答: