题目内容
已知25℃时,已知25℃时,CH3COOH的电离常数为2×10-5,该温度下,将0.10mol CH3COONa 固体溶于一定量水中配成溶液,在向该溶液中滴加0.1mol?L-1 的CH3COOH溶液,当溶液恰好呈中性时,加入的CH3COOH溶液的体积为 mL.
考点:弱电解质在水溶液中的电离平衡
专题:
分析:溶液呈中性,c(H+)=c(OH-)=10-7mol/L,设加入醋酸溶液体积为x,混合后溶液体积为V,则c(Na+)=c(CH3COO-)=
mol/L,结合电离平衡常数K=
计算.
| 0.10 |
| V |
| c(H+)c(CH3COO-) |
| c(CH3COOH) |
解答:
解:设加入醋酸溶液体积为x,混合后溶液体积为V,溶液呈中性,c(H+)=c(OH-)=10-7mol/L,c(Na+)=c(CH3COO-)=
mol/L,
K=
=
=2×10-5,
x=5×10-3L=5mL,
故答案为:5.
| 0.10 |
| V |
K=
| c(H+)c(CH3COO-) |
| c(CH3COOH) |
10-7×
| ||
|
x=5×10-3L=5mL,
故答案为:5.
点评:本题考查弱电解质的电离,为高频考点,侧重学生的分析能力和计算能力的考查,注意把握电离平衡常数的意义以及计算,难度不大.

练习册系列答案
相关题目
观察下列模型并结合有关信息进行判断,下列说法错误的是( )
| HCN | S8 | SF6分子 | B12结构单元 | |
| 结构模型示意图 |  |  |  |  |
| 备注 | / | 易溶于CS2 | / | 熔点1873K |
| A、HCN的结构式为H-C≡N |
| B、固态硫S8属于原子晶体 |
| C、SF6是由极性键构成的非极性分子 |
| D、单质硼属原子晶体,结构单元中含有30个B-B键 |
下列各化合物的命名中正确的是( )
A、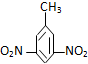 2,4-二硝基甲苯 2,4-二硝基甲苯 |
| B、(CH3CH2)2CHCH33-甲基戊烷 |
C、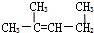 1,3-二甲基-2-丁烯 1,3-二甲基-2-丁烯 |
D、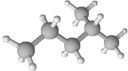 异戊烷 异戊烷 |
下列各组混合物的物质的量均为a mol,组内物质按任意比例混合,完全燃烧时消耗O2的物质的量不变的是( )
| A、甲醇、甲醛 |
| B、苯、1,3-丁二烯 |
| C、丙烯、2-丁烯 |
| D、乙醇、乙烯 |

 +CH3CH2OH→
+CH3CH2OH→ +HCl,写出草酰氯(分子式C2O2Cl2,分子结构式:
+HCl,写出草酰氯(分子式C2O2Cl2,分子结构式: )与足量有机物D反应的最终化学方程式
)与足量有机物D反应的最终化学方程式 ,由邻甲基苯酚--中间产物--有机物A,请选择正确中间产物(填B或C)
,由邻甲基苯酚--中间产物--有机物A,请选择正确中间产物(填B或C) C:
C:
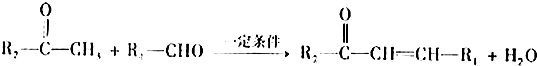

 .有机物X的键线式为:
.有机物X的键线式为: