题目内容
2.在NH3•H2O?NH4++OH-形成的平衡中,要使NH3•H2O的电离程度及[OH-]都增大,可采取的措施是( )| A. | 通入HCl | B. | 加少量NaOH固体 | C. | 加水 | D. | 升温 |
分析 氨水中存在下列平衡:NH3+H2O?NH3•H2O?NH4++OH-,加水促进电离,且如果加入能和铵根离子或氢氧根离子反应的物质,平衡就向电离方向移动,如果加入的物质中含有铵根离子或氢氧根离子,平衡向逆反应方向移动,以此解答该题.
解答 解:A、通入HCl,消耗氢氧根离子,电离程度增大,但是氢氧根离子的浓度减小,故A错误;
B、加NaOH,溶液中氢氧根离子浓度增大,平衡向逆反应方向移动,电离程度减小,故B错误;
C、加水,溶液浓度减小,电离程度增大,但是氢氧根离子的浓度减小,故C错误;
D、由于电离是吸热反应液,故升高温度,平衡右移,电离程度增大,氢氧根离子的浓度增大,故D正确;
故选D.
点评 本题考查了弱电解质的电离,注意把握影响弱电解质电离的因素,难度中等,注意加水稀释氨水电离平衡的移动,注意相关基础知识的积累.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
9.关于化学反应速率的说法正确的是( )
| A. | 化学反应速率可表示可逆反应进行的程度 | |
| B. | 化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 | |
| C. | 对于任何化学反应来说,反应速率越快,反应现象就越明显 | |
| D. | 根据反应速率的大小可知化学反应进行的相对快慢 |
10.M+N=Y+Z为吸热反应,对这个反应的下列说法中正确的是( )
| A. | X的能量一定低于M的,Y的能量一定低于N的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | Z和Y的总能量一定高于M和N的总能量 |
7.如图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).
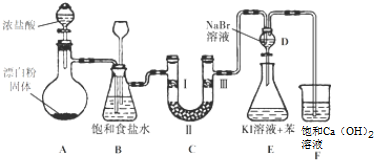
(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性.反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是E中溶液分为两层,上层(苯层)为紫红色,该现象不能(填“能”或“不能”)说明溴单质的氧化性强于碘,原因是氯气具有强氧化性,过量的氯气能够将碘离子氧化成碘单质,离子方程式为:Cl2+2I-=I2+2Cl-(用必要的文字和离子方程式回答).
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.

(1)装置A是氯气的发生装置,其中盛放浓盐酸的仪器名称是分液漏斗,请写出该反应相应的离子方程式:ClO-+2H++Cl-=Cl2↑++H2O.
(2)装置B中饱和食盐水的作用是除去Cl2中的HCl;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗中液面上升,形成水柱.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处依次放入物质的组合应是d(填字母编号).
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(5)此装置需要改进之处是:F原因是:氢氧化钙为微溶物,溶液中所含溶质较少,吸收氯气不充分,应改为氢氧化钠溶液吸收.
14.下列有关物质性质的比较顺序中,不正确的是( )
| A. | 热稳定性:H2O<H2S<H2Se | B. | 微粒半径:K+>Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 熔点:Li>Na>K>Rb |
7.在298K时,2molH2燃烧生成水蒸汽放出484kJ热量,下列热化学方程式正确的是( )
| A. | 2H2+O2=2H2O,△H=-484kJ/mol | B. | H2O(g)=H2(g)+$\frac{1}{2}$O2(g)△H=+242kJ/mol | ||
| C. | 2H2(g)+O2(g)=2H2O(l),△H=-484kJ/mol | D. | H2(g)+O2(g)=H2O(g)△H=+242kJ/mol |
14.能证明碳酸的酸性比硅酸强的事实是( )
| A. | 二氧化碳溶于水生成碳酸,二氧化硅不溶于水也不能跟水直接反应生成硅酸 | |
| B. | 在高温条件下,二氧化硅跟碳酸钠反应,生成硅酸钠和二氧化碳 | |
| C. | 二氧化硅的熔点比二氧化碳高 | |
| D. | 二氧化碳通入Na2SiO3稀溶液中,生成白色胶状沉淀 |
12.下列离子方程式中,正确的是( )
| A. | 把金属铁放入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 碳酸钡和稀硫酸反应:BaCO3+2H+=Ba2++CO2↑+H2O | |
| C. | 澄清石灰水和盐酸反应:H++OH-=H2O | |
| D. | 向CuSO4溶液中加入适量Ba(OH)2溶液:Ba2++SO42-=BaSO4↓ |