题目内容
14.能证明碳酸的酸性比硅酸强的事实是( )| A. | 二氧化碳溶于水生成碳酸,二氧化硅不溶于水也不能跟水直接反应生成硅酸 | |
| B. | 在高温条件下,二氧化硅跟碳酸钠反应,生成硅酸钠和二氧化碳 | |
| C. | 二氧化硅的熔点比二氧化碳高 | |
| D. | 二氧化碳通入Na2SiO3稀溶液中,生成白色胶状沉淀 |
分析 根据强酸制取弱酸判断酸性强弱,该反应必须在水溶液中进行,据此分析解答.
解答 解:A.溶解性与酸性强弱无关,不能通过溶解性判断酸性强弱,故A错误;
B.特殊条件下,SiO2与碳酸盐反应生成CO2不能证明碳酸酸性强于硅酸酸性,故B错误;
C.氧化物熔点高低与对应酸的酸性强弱无关,故C错误;
D.二氧化碳和水反应生成碳酸,碳酸和可溶性硅酸盐反应析出硅酸沉淀,说明碳酸能制取硅酸,所以能证明碳酸酸性强于硅酸酸性,故D正确;
故选:D.
点评 本题考查了酸的酸性强弱比较,熟悉强酸制取弱酸即可解答,题目不难.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
1.下列说法正确的是( )
| A. | 氢键不是化学键 | |
| B. | HF的稳定性很强,是因为其分子间能形成氢键 | |
| C. | 乙醇分子与水分子之间只存在范德华力 | |
| D. | 碘化氢的沸点比氯化氢的沸点高是由于碘化氢分子之间存在氢键 |
2.在NH3•H2O?NH4++OH-形成的平衡中,要使NH3•H2O的电离程度及[OH-]都增大,可采取的措施是( )
| A. | 通入HCl | B. | 加少量NaOH固体 | C. | 加水 | D. | 升温 |
9.下列化学方程式书写不正确的是( )
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | SiO2+H2O═H2SiO3 | ||
| C. | Cl2+2NaOH═NaCl+NaClO+H2O | D. | 2H2S+SO2═3S+2H2O |
6.对于反应:N2(g)+3H2(g)?2NH3(g),△H<0 的平衡体系,在其它条件不变时,采取下列措施,其中能既使正、逆反应速率增大,又能使反应物转化率增大的是( )
| A. | 增大体系压强 | B. | 升温 | C. | 加入铁触媒 | D. | 减小NH3的浓度 |
3.火法冶铜涉及反应:2Cu2O+Cu2S$\frac{\underline{\;高温\;}}{\;}$6Cu+SO2↑,有关该反应的说法正确的是( )
| A. | 属于置换反应 | B. | 铜的化合价升高 | C. | 反应转移4e | D. | 还原剂是Cu2O |
4.下列为某同学根据中学化学教材中的数据所做的判断,其中错误的是( )
| A. | 根据Ksp数据,判断长时间煮沸Mg(HCO3)2溶液所得沉淀是MgCO3还是Mg(OH)2 | |
| B. | 根据反应热数据,判断不同反应的反应速度的大小 | |
| C. | 根据Kc数据,判断某可逆反应在某一温度下是否达到平衡 | |
| D. | 根据Ka数据,判断弱酸的酸性强弱 |
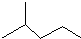 表示的分子式C6H14;名称是2-甲基戊烷.
表示的分子式C6H14;名称是2-甲基戊烷.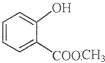 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.