题目内容
16.若能发现第117号元素X,它的原子结构与卤族元素相似,电子排布有7个电子层,且最外层有7个电子.下列叙述中正确的是( )| A. | 此X元素的气态氢化物的化学式为HX,在常温很稳定 | |
| B. | 其单质带有金属光泽,具有强氧化性,可与KI发生置换反应生成I2 | |
| C. | 其单质的分子式为X2,易溶于有机溶剂 | |
| D. | AgX是一种有色的易溶于水的化合物 |
分析 117号元素X,它的原子结构与卤族元素相似,电子排布有7个电子层,且最外层有7个电子,该元素处于处于ⅦA族.
A.元素非金属性越强,对应氢化物越稳定;
B.同主族自上而下非金属性减弱,金属性增强;
C.与氯气、溴、碘的结构与性质相似;
D.AgCl、AgBr、AgI溶解性依次减小.
解答 解:117号元素X,它的原子结构与卤族元素相似,电子排布有7个电子层,且最外层有7个电子,该元素处于处于ⅦA族.
A.同主族自上而下非金属性减弱,117号元素非金属性比At弱,元素非金属性越强,对应氢化物越稳定,该元素氢化物稳定性比HAt差,故该氢化物HX不稳定,故A错误;
B.同主族自上而下非金属性减弱,金属性增强,其单质带有金属光泽,氧化性比碘的弱,不能与KI发生置换反应生成I2,故B错误;
C.处于ⅦA族,与氯气、溴、碘的结构与性质相似,其单质的分子式为X2,易溶于有机溶剂,故C正确;
D.处于ⅦA族,AgCl、AgBr、AgI溶解性依次减小,颜色加深,AgX是一种有色的难溶于水的化合物,故D错误,
故选:C.
点评 本题考查元素周期律应用,注意理解同主族元素单质化合物相似性与递变性,注意掌握卤素单质化合物性质.

练习册系列答案
相关题目
7.向含NaBr、NaCl、NaI的混合溶液中通入足量的氯气,充分反应后,将溶液加热蒸干、灼烧,最终获得的残留固体可能是( )
| A. | NaCl NaI | B. | NaCl、I2 | C. | NaCl | D. | NaCl、NaBr、I2 |
4.化学与日常生活密切相关,下列说法错误的是( )
| A. | Al2O3可用作高温耐火材料 | |
| B. | 利用漂白粉的氧化性漂白织物 | |
| C. | 浓硫酸可刻蚀石英制艺术品 | |
| D. | 在医疗上碳酸氢钠可用于治疗胃酸过多 |
11.下列各组离子,在某无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | K+、Na+、SO4-、HCO3- | B. | K+、Cu2+、SO4-、NO3- | ||
| C. | K+、Na+、Cl-、NO3- | D. | K+、Fe3+、NO3-、Cl- |
1.我国最近在太阳能光电催化-化学耦合分解硫化氢研究中获得新进展,相关装置如图所示.下列说法正确的是( )

| A. | 该制氢工艺中光能最终转化为化学能 | |
| B. | 该装置工作时,H+由a极区流向b极区 | |
| C. | b极上发生的电极反应为Fe3++e-═Fe2+ | |
| D. | b极区需不断补充含Fe3+和Fe2+的溶液 |
8.可用于区别溴蒸气和N02气体的试剂是( )
| A. | KI淀粉溶液 | B. | 蒸馏水 | C. | AgNO3溶液 | D. | NaOH溶液 |
5.X、Y、Z、M 是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z 相邻.X的核电荷数是Y的核外电子数的一半,Y与M 可形成化合物M2Y.下列说法正确的是( )
| A. | 原子半径:Z>Y | |
| B. | 简单离子的半径:M的离子>Z的离子>Y的离子>X的离子 | |
| C. | X的阴离子和Y的阴离子核外电子数相同 | |
| D. | Z元素的最高价氧化物的水化物的化学式为HZO4 |

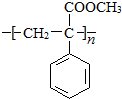 、
、 .
. +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$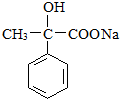 +NaBr+H2O.
+NaBr+H2O.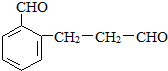 等.
等.