题目内容
下列装置所示的实验中,能达到实验目的是( )
A、 验证NaHCO3和Na2CO3热稳定性大 |
B、 分离乙醇与水的混合物 |
C、 除去Cl2中的HCl |
D、 排水法收集氧气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碳酸氢钠应放在套装小试管中;
B.乙醇和水互溶;
C.氯气和氯化氢都能与氢氧化钠反应;
D.氧气不溶于水.
B.乙醇和水互溶;
C.氯气和氯化氢都能与氢氧化钠反应;
D.氧气不溶于水.
解答:
解:A.套装小试管加热温度较低,碳酸氢钠应放在套装小试管中,通过澄清水是否变浑浊可证明稳定性,故A错误;
B.乙醇和水互溶,不能用分液漏斗分离,故B错误;
C.氯气和氯化氢都能与氢氧化钠反应,将原物质除掉,故C错误;
D.氧气不溶于水,可用排水法收集,故D正确.
故选D.
B.乙醇和水互溶,不能用分液漏斗分离,故B错误;
C.氯气和氯化氢都能与氢氧化钠反应,将原物质除掉,故C错误;
D.氧气不溶于水,可用排水法收集,故D正确.
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及碳酸钠与碳酸氢钠的稳定性比较、物质分离与提纯以及气体收集等,侧重实验基本操作和实验原理的考查,注意装置的作用及实验的操作性、评价性分析,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
常温下,下列溶液中的微粒浓度关系正确的是( )
| A、新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) |
| B、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、10-3 mol?L-1的氨水与pH=3的硫酸等体积混合:c(SO42-)=c(NH4+)>c(OH-)=c(H+) |
| D、0.1mol?L-1CH3COOH溶液与0.1mol?L-1NaOH溶液等体积混合:c(Na+)=c(CH3COO-)+c(CH3COOH) |
下列实验能成功的是( )
| A、5mL苯与1mL浓溴水反应(Fe粉作催化剂)制溴苯 |
| B、2.5g苯酚与2.5mL40%的甲醛溶液混合,沸水浴加热制酚醛树脂 |
| C、加热5mL溴乙烷和15mL20%的KOH水溶液,使其充分反应.在反应所得溶液中加入4-5滴AgNO3溶液,经检验溴乙烷中的溴 |
| D、在试管中依次加放2mL蒸馏水、4mL浓硫酸、2mL95%的乙醇、3gNaBr粉末,加热制溴乙烷 |
用蒸馏水稀释0.1mol/L的CH3COOH时,始终保持增大趋势的是( )
| A、c(CH3COOH) |
| B、c(H+) |
| C、c(OH-) |
| D、c(CH3COO-) |
对于化学反应A+B=C+D的下列说法中,正确的是( )
| A、若C、D分别为单质和化合物,则该反应一定是置换反应 |
| B、若C、D分别为盐和水,则该反应一定是中和反应 |
| C、若A、B、C、D都是化合物,该反应一定是复分解反应 |
| D、若A为碱溶液,B为盐溶液,则C和D可能是两种沉淀 |
14g NaHCO3和7.8g Na2O2混合后放在密闭容器中加热使之充分反应,然后趁热排出气体物质,则容器中残留物的成分是( )
| A、Na2O2和NaHCO3 |
| B、NaHCO3和Na2CO3 |
| C、NaOH和Na2CO3 |
| D、只有Na2CO3 |
凤岗的“富锌富硒”茶现已享誉全国,富含硒元素,有延年益寿、抗衰老等作用.二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3、浓H2SO4反应生成SeO2以回收Se.在回收过程当中涉及到如下两个化学反应①SeO2+4KI+4HNO3=Se+2I2+4KNO3+2H2O;②Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O,下列有关叙述正确的是( )
| A、SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2 |
| B、①中Se是氧化产物,I2是还原产物 |
| C、反应①中KI是氧化剂,SeO2是还原剂 |
| D、反应①中每有1.0 mol I2生成,转移电子数目为4NA |
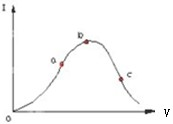 醋酸是一种弱电解质.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答:
醋酸是一种弱电解质.在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示.请回答: