题目内容
14g NaHCO3和7.8g Na2O2混合后放在密闭容器中加热使之充分反应,然后趁热排出气体物质,则容器中残留物的成分是( )
| A、Na2O2和NaHCO3 |
| B、NaHCO3和Na2CO3 |
| C、NaOH和Na2CO3 |
| D、只有Na2CO3 |
考点:钠的重要化合物,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:Na2O2与等物质的量的NaHCO3混合后,在密闭容器中充分加热,可能发生的反应有:2NaHCO3
Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,CO2+2NaOH=Na2CO3+H2O,根据二者的物质的量的关系来判断残留固体.
| ||
解答:
解:14g碳酸氢钠的物质的量约为0.17mol;7.8g 过氧化钠的物质的量为0.1mol;
2NaHCO3
Na2CO3+CO2↑+H2O;
2 1 1 1
0.17mol 0.085mol 0.085mol 0.085mol
2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
2 2 2 4
0.085mol 0.085mol 0.015mol 0.085mol
所以过氧化钠完全反应,剩余故体为碳酸钠和氢氧化钠的混合物;
故选:C.
2NaHCO3
| ||
2 1 1 1
0.17mol 0.085mol 0.085mol 0.085mol
2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
2 2 2 4
0.085mol 0.085mol 0.015mol 0.085mol
所以过氧化钠完全反应,剩余故体为碳酸钠和氢氧化钠的混合物;
故选:C.
点评:本题考查钠的化合物的性质,题目难度不大,本题注意等物质的量的NaHCO3和Na2O2固体混合物的特点,注意有关反应,以正确判断最终产物.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
下列各组离子在指定的环境中一定能大量存在的是( )
| A、pH=1的溶液中:S2O32-、Cu2+、Na+、Cl- |
| B、能使酚酞变红色的溶液中:Na+、K+、S2-、HCO3- |
| C、加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3- |
| D、使甲基橙变黄色的溶液中:Na+、K+、Cl-、SO42- |
下列装置所示的实验中,能达到实验目的是( )
A、 验证NaHCO3和Na2CO3热稳定性大 |
B、 分离乙醇与水的混合物 |
C、 除去Cl2中的HCl |
D、 排水法收集氧气 |
常温下,0.1mol?L-1某一元碱(AOH)溶液中
=1×108,下列说法正确的是( )
| C(OH-) |
| C(H+) |
| A、该一元碱(AOH)溶液的pH=13 |
| B、该溶液中水电离出的C(OH-)=10-3 mol?L-1 |
| C、将pH=1的盐酸溶液V1 L与0.1 mol?L-1 AOH溶液V2 L混合,若混合溶液pH=7,则V1=V2 |
| D、将pH=1的盐酸溶液V1L与0.1 mol?L-1 AOH溶液V2 L混合,若混合溶液pH>7,则溶液中离子浓度由大到小的顺序可能为C(A+)>C(Cl-)>C(OH-)>C(H+) |
已知,单质碘受热易升华.从海带中提取碘的实验过程中,涉及下列实验操作步骤,关于各步骤的实验目的或实验操作,描述正确的是( )
A、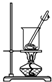 将海带灼烧成灰 |
B、 过滤得含I-的溶液 |
C、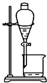 下层放出碘的苯溶液 |
D、 分离碘并回收苯 |
化学与环境、生产、生活密切相关,下列说法不正确的是( )
| A、成都加快建设地铁、轻轨,减少汽车尾气排放,符合“低碳经济”要求 |
| B、绿色化学的核心是应用化学原理对环境污染进行治理 |
| C、用浸泡过高锰酸钾溶液的硅土吸收水果释放的乙烯,有利于水果保鲜 |
| D、明矾水溶液中的氢氧化铝胶体能吸附水中悬浮物,达到净水目的 |
区分晶体和非晶体最可靠的科学方法是( )
| A、测定熔、沸点 |
| B、观察外形 |
| C、对固体进行X射线衍射 |
| D、通过比较硬度确定 |
下列说法中正确的是( )
| A、在电解池中,与电源正极相连的电极是阴极 |
| B、在电解池中,物质在阴极发生氧化反应 |
| C、在原电池中,物质在负极发生氧化反应 |
| D、在原电池中,电子在正极流向负极 |
恒温下,将1mol N2和3mol H2在体积为2L的容器中混合,发生如下反应:N2(g)+3H2(g)?2NH3(g),2s时测得NH3的体积分数为25%.则下列说法中不正确的是( )
| A、用N2浓度的减少表示的平均反应速率为0.2 mol?L-1?s-1 |
| B、2 s时N2的转化率为40% |
| C、2 s时混合气体中n(N2)?n(H2)?n(NH3)=3:9:4 |
| D、2 s 时NH3的浓度为0.4 mol?L-1 |