题目内容
8.下列粒子中不能大量共存的是( )| A. | NH4+、Al3+、SO42-、NO3- | B. | Al3+、K+、Cl-、S2- | ||
| C. | NH4+、Cl-、K+、CO32- | D. | Ca2+、NO3-、HCO3-、Al3+ |
分析 根据离子之间不能结合生成沉淀、气体、水等,不能相互促进水解等,则离子大量共存,以此来解答.
解答 解:A.该组离子之间不反应,可大量共存,故A不选;
B.Al3+、S2-相互促进水解,不能共存,故B选;
C.该组离子之间不反应,可大量共存,故C不选;
D.HCO3-、Al3+相互促进水解,不能共存,故D不选;
故选BD.
点评 本题考查离子的共存,为高频考点,把握离子之间的反应为解答本题的关键,侧重分析与应用的考查,注意水解反应的应用,题目难度不大.

练习册系列答案
相关题目
15.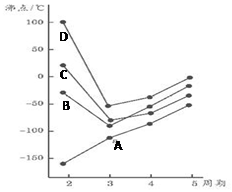 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )
如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )
 如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )
如图为四、五、六、七主族元素简单氢化物沸点随周期变化图象,(A、B、C、D代表氢化物中另外一种元素)分析图象,下列说法正确的是( )| A. | A元素氧化物晶体中存在分子间作用力 | |
| B. | A、B、C、D非金属性由小到大的顺序是:A<B<D<C | |
| C. | D的氢化物固态比液态时密度大 | |
| D. | B元素一种氢化物可做火箭的染料,为CH4 |
13. 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
 将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )
将Na2O2加入含有Al3+、Fe2+的混合液中并微热,产生沉淀和气体的物质的量(mol)与加入Na2O2的物质的量(mol)的关系如图所示.下列说法不正确的是( )| A. | a=1.75 | |
| B. | b=0.5 | |
| C. | 原溶液中Al3+与Fe2+的物质的量之比为1:2 | |
| D. | 最后得到的沉淀为Fe(OH)3 |
13.下列有关sp杂化轨道的叙述正确的是( )
| A. | 是由一个1s轨道和一个2p轨道线性组合而成 | |
| B. | 等性sp杂化轨道中所含s、p的成分一样 | |
| C. | 等性sp杂化轨道有两个,一个能量升高,另一个能量降低,但总能量保持不变 | |
| D. | sp杂化轨道可与其他原子轨道形成σ键和π键 |
20.下列物质属于电解质的是( )
| A. | Cl2 | B. | KNO3 | C. | SO2 | D. | Al |
17.高炉炼铁中生成铁的反应一定是( )
| A. | 氧化还原反应 | B. | 置换反应 | C. | 复分解反应 | D. | 分解反应 |
18.室温下,pH=4的盐酸和pH=10的氨水等体积混合后,所得溶液的pH值( )
| A. | 一定大于7 | B. | 一定等于7 | C. | 一定小于7 | D. | 可能大于7 |