题目内容
7.电化学降解法可用于治理水中硝酸盐的污染,其工作原理如图所示.下列说法正确的是( )
| A. | A极为负极,电子从铂电极流向该极 | |
| B. | Pt电极上发生还原反应 | |
| C. | Ag-Pt电极发生的反应是:2NO3-+6H2O+10e-═N2↑+12OH- | |
| D. | 电解一段时间后,两地减少的质量一样多 |
分析 A.该装置中,硝酸根离子得电子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,连接阳极的电极为正极;
B.阳极上水失电子发生氧化反应;
C.阴极上硝酸根离子得电子发生还原反应;
D.根据转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室计算.
解答 解:A.根据图知,电解槽右边部分N元素化合价由+5价变为0价,所以硝酸根离子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,所以A是正极、B是负极,故A错误;
B.Pt电极为阳极,阳极上水失电子生成氢离子和氧气而发生氧化反应,故B错误;
C.Ag-Pt电极为阴极,阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3-+6H2O+10e-═N2↑+12OH-,故C正确;
D.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3-+6H2O+10e-═N2↑+12OH-,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故电解一段时间后,两极减少的质量不同,故D错误;
故选C.
点评 本题考查了电解原理,根据N元素化合价变化确定阴阳极、正负极,难点是电极反应式的书写,易错选项是D,注意氢离子还进入阴极室,很多同学往往只考虑析出的气体而导致错误,为易错点.

练习册系列答案
相关题目
17.乙基香草醛(结构为 )的同分异构体有多种.符合下列条件的同分异构体有( )种
)的同分异构体有多种.符合下列条件的同分异构体有( )种
①能与NaHCO3溶液反应 ②遇FeCl3溶液显紫色且能与浓溴水反应
③苯环上有两个烃基 ④苯环上的官能团处于对位.
 )的同分异构体有多种.符合下列条件的同分异构体有( )种
)的同分异构体有多种.符合下列条件的同分异构体有( )种①能与NaHCO3溶液反应 ②遇FeCl3溶液显紫色且能与浓溴水反应
③苯环上有两个烃基 ④苯环上的官能团处于对位.
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
15.草木灰中可能含K2CO3、K2SO4及NaCl等盐,将草木灰用蒸馏水浸取得浸取液进行实验,下列根据现象得出的结论不正确的是( )
| A. | 向浸取液中加入BaCl2有白色沉淀,不能说明其中含有SO42- | |
| B. | 向浸取液中加入AgNO3溶液有白色沉淀,说明其中含有Cl- | |
| C. | 洁净铂丝蘸取浸取液少许,在酒精灯火焰上灼烧,火焰呈黄色,不能确定是否含K+ | |
| D. | 向浸取液中滴加稀硫酸,产生无色无味的气体,说明其中含有CO32- |
2.下列各式表示水解反应的是( )
| A. | HCO3-+H2O?H3O++CO32- | B. | HS-+H2O?H2S+OH- | ||
| C. | Fe3++3H2O?Fe(OH)3↓+3H+ | D. | Br-+H2O?HBr+OH- |
12.表是一些共价键的键能(kJ/mol)数据,以下表达中肯定正确的是( )
| 共价键 | 键能 | 共价键 | 键能 |
| H-H | 436 | H-F | 565 |
| C-F | 427 | H-S | 339 |
| C-C1 | 330 | H-Se | 314 |
| A. | H2(g)→2H(g)△H=+436kJ/mol | |
| B. | 键长越短,共价键越牢固 | |
| C. | 相同条件下CH3F比CH3C1更易发生水解反应 | |
| D. | 相同压强下,H2S的沸点比H2Se的沸点高 |
19.五氧化二氮(N2O5)是有机合成中常用的绿色硝化剂,可用NO2与O3反应制得.某化学兴趣小组设计如下实验装置制备N2O5(部分装置略去).

(1)铜和浓硝酸反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.加入浓硝酸后,装置Ⅰ中烧瓶上部可观察到的现象是有红棕色气体生成.
(2)仪器a的名称为球形干燥管,该仪器中盛装的试剂是D(填标号).
A.生石灰B.浓硫酸C.碱石灰D.五氧化二磷
(3)已知下列物质的有关数据.
装置Ⅱ中持续通入O3,为得到尽可能多的纯净的N2O5,温度控制在24℃〜32℃.收集到的N2O5固体中含有液态物质,可能原因是干燥不完全,导致有硝酸生成.
(4)装置Ⅲ的作用是安全瓶,防止倒吸.
(5)化学兴趣小组用制得的N2O5制备少量对硝基甲苯( ,相对分子质量137).步骤如下:在三口烧瓶中放入催化剂和30mL N2O5的CH2Cl2溶液(N2O5的浓度为lmol•L-1),30℃时,滴加15mL甲苯,充分反应得对硝基甲苯 1.73g.回答下列问题:
,相对分子质量137).步骤如下:在三口烧瓶中放入催化剂和30mL N2O5的CH2Cl2溶液(N2O5的浓度为lmol•L-1),30℃时,滴加15mL甲苯,充分反应得对硝基甲苯 1.73g.回答下列问题:
①制备对硝基甲苯的化学方程式为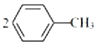 +N2O5$→_{△}^{催化剂}$
+N2O5$→_{△}^{催化剂}$ +H2O.
+H2O.
②N2O5生成对硝基甲苯的转化率为21.05%.

(1)铜和浓硝酸反应的离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.加入浓硝酸后,装置Ⅰ中烧瓶上部可观察到的现象是有红棕色气体生成.
(2)仪器a的名称为球形干燥管,该仪器中盛装的试剂是D(填标号).
A.生石灰B.浓硫酸C.碱石灰D.五氧化二磷
(3)已知下列物质的有关数据.
| 物质 | 熔点/℃ | 沸点/℃ |
| N2O5 | 41 | 32 (升华) |
| N2O4 | -11 | 24 |
(4)装置Ⅲ的作用是安全瓶,防止倒吸.
(5)化学兴趣小组用制得的N2O5制备少量对硝基甲苯(
 ,相对分子质量137).步骤如下:在三口烧瓶中放入催化剂和30mL N2O5的CH2Cl2溶液(N2O5的浓度为lmol•L-1),30℃时,滴加15mL甲苯,充分反应得对硝基甲苯 1.73g.回答下列问题:
,相对分子质量137).步骤如下:在三口烧瓶中放入催化剂和30mL N2O5的CH2Cl2溶液(N2O5的浓度为lmol•L-1),30℃时,滴加15mL甲苯,充分反应得对硝基甲苯 1.73g.回答下列问题:①制备对硝基甲苯的化学方程式为
 +N2O5$→_{△}^{催化剂}$
+N2O5$→_{△}^{催化剂}$ +H2O.
+H2O.②N2O5生成对硝基甲苯的转化率为21.05%.
16.氢氰酸(HCN)是一种具有苦杏仁气味的无色液体,易溶于水.回答下列问题:
(1)一定的温度和催化剂作用下,利用甲烷、氨气为原料氧化合成氢氰酸.
①氨气的电子式为 .
.
②合成氢氰酸的化学方程式为2CH4+2NH3+3O2$\frac{\underline{\;一定条件\;}}{催化剂}$2HCN+6H2O
(2)已知25℃时HCN和H2CO3的电离常数(Ka)如表:
25℃时,物质的量浓度均为0.1mol•L-1的NaCN、NaHCO3和Na2CO3三种溶液,其pH最大的是Na2CO3(填化学式).
(3)-定条件下,HCN与H2和H2O反应如下:
I.HCN(g)+3H2(g)?NH3(g)+CH4(g)△H1
Ⅱ.HCN(g)+H2O(g)?NH3(g)+CO(g)△H2
①反应Ⅲ,CO(g)+3H2(g)?CH4(g)+H2O(g)的△H=△H1-△H2 (用△H1、△H2表示).
②对于反应Ⅱ,减小压强,HCN的转化率不变(填“提高”、“不变”或“降低”).
③反应I、Ⅱ的平衡常数对数值(lgK)与温度的关系如图甲所示,则T1K时,反应Ⅲ的平衡常数对数值lgK=10.

(4)电解法处理含氰废水的原理如图乙所示,阳极CN-先发生电极反应:CN-+2OH--2e-═CNO-+H2O,CNO-在阳极上进一步氧化的电极反应式为2CNO-+4OH--6e-=N2↑+2CO2↑+2H2O.
(1)一定的温度和催化剂作用下,利用甲烷、氨气为原料氧化合成氢氰酸.
①氨气的电子式为
 .
.②合成氢氰酸的化学方程式为2CH4+2NH3+3O2$\frac{\underline{\;一定条件\;}}{催化剂}$2HCN+6H2O
(2)已知25℃时HCN和H2CO3的电离常数(Ka)如表:
| 物质 | 电离常数(Ka) |
| HCN | Ka=5×10-10 |
| H2CO3 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
(3)-定条件下,HCN与H2和H2O反应如下:
I.HCN(g)+3H2(g)?NH3(g)+CH4(g)△H1
Ⅱ.HCN(g)+H2O(g)?NH3(g)+CO(g)△H2
①反应Ⅲ,CO(g)+3H2(g)?CH4(g)+H2O(g)的△H=△H1-△H2 (用△H1、△H2表示).
②对于反应Ⅱ,减小压强,HCN的转化率不变(填“提高”、“不变”或“降低”).
③反应I、Ⅱ的平衡常数对数值(lgK)与温度的关系如图甲所示,则T1K时,反应Ⅲ的平衡常数对数值lgK=10.

(4)电解法处理含氰废水的原理如图乙所示,阳极CN-先发生电极反应:CN-+2OH--2e-═CNO-+H2O,CNO-在阳极上进一步氧化的电极反应式为2CNO-+4OH--6e-=N2↑+2CO2↑+2H2O.
14.分子式为C8H8O2的属于酯类的芳香族化合物共有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
 .
.