题目内容
下面是一些原子的2p能级和3d能级中电子在原子轨道上的排布情况,其中正确的是( )
A、 |
B、 |
C、 |
D、 |
考点:原子核外电子排布,原子核外电子的能级分布
专题:原子组成与结构专题
分析:原子核外电子排布,应满足能量最低原理,洪特规则以及泡利不相容原理,以此进行判断.
解答:
解:A.同一轨道自旋方向相同,违反泡利不相容原理,故A错误;
B.2p能层有3个电子,应在3个不同的轨道,不符合洪特规则,故B错误;
C.3d能级有8个电子,应在5个不同的轨道,违反了洪特规则,故C错误;
D.符合洪特规则、泡利不相容原理,故D正确.
故选D.
B.2p能层有3个电子,应在3个不同的轨道,不符合洪特规则,故B错误;
C.3d能级有8个电子,应在5个不同的轨道,违反了洪特规则,故C错误;
D.符合洪特规则、泡利不相容原理,故D正确.
故选D.
点评:本题考查原子核外电子排布,题目难度不大,本题注意把握核外电子的排布规律即可解答该题.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
锌片与2mol/L H2SO4反应制取氢气时,下列措施能使氢气生成速率加快的是( )
| A、向反应体系中加入5mol/L的硝酸溶液提高氢离子浓度 |
| B、将稀H2SO4改用98%浓H2SO4 |
| C、向反应体系中立即加入大量CuSO4溶液 |
| D、向反应体系中加入4.5mol/L的盐酸溶液 |
下列关于物质性质变化的比较不正确的是( )
| A、酸性:HNO3>H3PO4>H2SiO3 |
| B、碱性:LiOH<NaOH<KOH |
| C、原子半径:O<S<Na |
| D、还原性:I-<Cl-<F- |
设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、等质量的N2和CO所含分子数均为NA |
| B、1 mol?L-1NaCl溶液含有Cl-的个数为NA |
| C、常温常压下48gO2和48gO3含有的氧原子数均为3NA |
| D、标准状况下,22.4 L水中含有NA个H2O分子 |
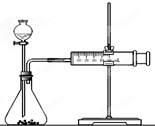 影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.