题目内容
19.周期表中前36号元素A、B、C、D、E、F、G、H,它们的原子序数依次增大,其中B、C、D为同一周期;E、F、G为同一周期;A和E、D和G分别为同一主族;A与B组成的化合物是一种温室气体;D元素原子的最外层电子数是次外层电子数的3倍;E是所在周期原子半径最大的元素(除稀有气体外);F元素的离子半径是同周期元素形成的简单离子中最小的;H元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子.(1)H在周期表中的位置为第四周期IB族,常温下,0.1mol/LE的最高价氧化物对应水化物的溶液与0.1mol/LG的最高价氧化物对应水化物溶液按体积比1:2混合后,溶液的pH=1.
(2)一定条件下,A2气体与C2气体充分反应可生成6.8g的气体,放出18.44kJ热量,则该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol.
(3)C和E组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式 是Na3N+4H2O=3NaOH+NH3•H2O.
(4)用惰性电极电解FCl3溶液,阴极区的现象为有白色沉淀生成,有无色气体产生,用离子方程式解释产生该现象的原因:2Al3++6H2O=3H2↑+2Al(OH)3↓.
分析 周期表中前36号元素A、B、C、D、E、F、G、H,它们的原子序数依次增大;D元素原子的最外层电子数是次外层电子数的3倍,D原子只能有2个电子层,最外层电子数为6,则D为氧元素;H元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则H原子核外电子数=2+8+18+1=29,则H为Cu元素;D和G分别为同一主族,G的原子序数小于Cu,则G为硫元素;E是所在周期原子半径最大的元素(除稀有气体外),处于ⅠA族,结合原子序数可知,E只能处于第三周期,故E为Na;F元素的离子半径是同周期元素形成的简单离子中最小的,原子序数介于Na与硫之间,故F为Al;A和E同主族,A与B组成的化合物是一种温室气体,B、C、D为同一周期,则A为氢元素,B为碳元素,C的原子序数介于碳、氧之间,故C为氮元素,据此解答.
解答 解:周期表中前36号元素A、B、C、D、E、F、G、H,它们的原子序数依次增大;D元素原子的最外层电子数是次外层电子数的3倍,D原子只能有2个电子层,最外层电子数为6,则D为氧元素;H元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,则H原子核外电子数=2+8+18+1=29,则H为Cu元素;D和G分别为同一主族,G的原子序数小于Cu,则G为硫元素;E是所在周期原子半径最大的元素(除稀有气体外),处于ⅠA族,结合原子序数可知,E只能处于第三周期,故E为Na;F元素的离子半径是同周期元素形成的简单离子中最小的,原子序数介于Na与硫之间,故F为Al;A和E同主族,A与B组成的化合物是一种温室气体,B、C、D为同一周期,则A为氢元素,B为碳元素,C的原子序数介于碳、氧之间,故C为氮元素.
(1)H为Cu,处于周期表中第四周期IB族,
常温下,0.1mol/L NaOH溶液与0.1mol/硫酸溶液按体积比1:2混合后,混合溶液溶液呈酸性,混合后溶液中氢离子浓度为$\frac{0.1mol/L×2L×2-0.1mol/L×1L}{2L+1L}$=0.1mol/L,溶液的pH=-lg0.1=1,
故答案为:第四周期IB族;1;
(2)一定条件下,H2气体与N2气体充分反应可生成6.8g的气体,放出18.44kJ热量,则生成2mol氨气放出的热量=18.44kJ×$\frac{2mol×17g/mol}{6.8g}$=92.2kJ,则该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol,
故答案为:N2(g)+3H2(g)?2NH3(g)△H=-92.2kJ/mol;
(3)N和Na组成的一种离子化合物,能与水反应生成两种碱,应生成氢氧化钠与一水合氨,该化合物为Na3N,该反应的化学方程式是:Na3N+4H2O=3NaOH+NH3•H2O,
故答案为:Na3N+4H2O=3NaOH+NH3•H2O;
(4)用惰性电极电解AlCl3溶液,阳极为氯离子放电生成氯气,阴极氢离子得到电子生成氢气,生成的氢氧根离子与铝离子反应生成氢氧化铝沉淀,阴极离子方程式为:2Al3++6H2O=3H2↑+2Al(OH)3↓,阴极现象为:有白色沉淀生成,有无色气体产生,
故答案为:有白色沉淀生成,有无色气体产生;2Al3++6H2O=3H2↑+2Al(OH)3↓.
点评 本题考查结构性质位置关系应用,推断元素是解题关键,涉及核外电子排布、溶液pH计算、热化学方程式、电解原理等,难度中等,侧重考查学生对基础知识掌握与迁移应用.

| A. | N4与N2互为同位素 | |
| B. | N4H44+与NaOH溶液反应的离子方程式为N4H44++4OH-═N4+4H2O | |
| C. | N4H4(SO4)2为弱电解质 | |
| D. | N4H44+中只含有极性共价键,不含非极性共价键 |
| A. | 6.5g金属Zn与过量的硫酸反应,硫酸无论浓稀,转移电子数均为0.2Na | |
| B. | 含有1mol FeCl3的溶液中阴离子数等于3NA | |
| C. | 惰性电极电解食盐水,若线路中通过NA电子电量,则阳极产生气体11.2L | |
| D. | Na2S和Na2O2 固体混合物15.6g中,含有的阴离子数为0.3NA |
| A. | K+、NO3-、OH-、Cl- | B. | Cu2+、SO42-、H+、Na+ | ||
| C. | H+、Ba2+、Mg2+、NO3- | D. | NH4+、MnO4-、H+、K+ |
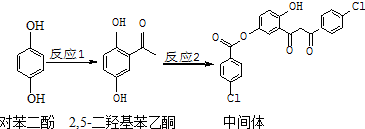
| A. | 对苯二酚在空气中能稳定存在 | |
| B. | 1 mol该中间体最多可与11 mol H2反应 | |
| C. | 2,5-二羟基苯乙酮能发生加成、取代、缩聚反应 | |
| D. | 该中间体分子中含有1个手性碳原子 |
| A. | 丁烷的结构简式为CH3CH2CH2CH3 | B. | 一氯乙烷的结构式为CH3Cl | ||
| C. | 四氯化碳的电子式为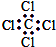 | D. | 苯的分子式为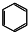 |
| A. | 原子序数为55 | B. | 电子数是55 | C. | 中子数是137 | D. | 质量数是137 |
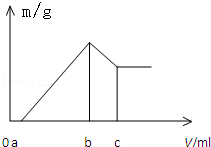 将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:
将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算: