题目内容
8.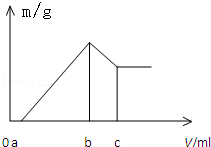 将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:
将镁、铝的混合物0.1mol 溶于100mL 2mol/L H2SO4溶液中,然后再滴加1mol/L 的NaOH溶液,沉淀质量m 随加入NaOH溶液的体积V 变化情况如图所示,计算:(1)当加入bml NaOH溶液时产生的沉淀物的化学式为Al(OH)3、Mg(OH)2
(2)当a=120mL时,金属混合物中n(Mg)=0.02mol,n(Al)=0.08mol,c=480mL;
(3)若欲使Mg2+、Al3+刚好完全沉淀,则加入的NaOH的体积V应为400毫升.
分析 (1)b点为沉淀量最大时,沉淀为Al(OH)3、Mg(OH)2;
(2)当a=120mL时,根据图象可知,在滴加NaOH溶液到体积120mL过程中,没有沉淀生成,说明硫酸有剩余,滴加的NaOH用于中和剩余硫酸,120mL时,剩余的H2SO4与滴加的NaOH恰好完全反应,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,令MgSO4为xmol,Al2(SO4)3为ymol,根据守恒列方程求算n(Mg)、n(Al);
当滴加NaOH溶液到体积c时,Al(OH)3完全溶解,沉淀是Mg(OH)2,溶液是Na2SO4和NaAlO2混合液,根据守恒,有n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al),据此求出n(NaOH),再利用V=$\frac{n}{c}$计算;
(3)当溶液中Mg2+、Al3+恰好沉淀完全时,即沉淀达到最大值,此时溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有n(Na+)=2n(Na2SO4)=2(H2SO4),据此求出n(NaOH),再利用V=$\frac{n}{c}$计算.
解答 解:(1)b点为沉淀量最大时,沉淀为Al(OH)3、Mg(OH)2,
故答案为:Al(OH)3、Mg(OH)2;
(2)当a=120mL时,根据图象可知,在滴加NaOH溶液到体积120mL过程中,没有沉淀生成,说明硫酸有剩余,滴加的NaOH用于中和剩余硫酸,120mL时,剩余的H2SO4与滴加的NaOH恰好完全反应,溶液是MgSO4、Al2(SO4)3和Na2SO4混合液,
由Na+离子守恒可知,n(Na2SO4)=$\frac{1}{2}$n(NaOH)=$\frac{1}{2}$×0.12L×1mol/L=0.06mol
令MgSO4为xmol,Al2(SO4)3为ymol,则:
根据Mg原子、Al原子守恒有:x+2y=0.1
根据SO42-离子守恒有:x+3y=0.1×2-0.06
联立方程,解得:x=0.02、y=0.04
所以金属粉末中n(Mg)=0.02mol,n(Al)=2y=2×0.04mol=0.08mol,
当滴加NaOH溶液到体积c时,Al(OH)3完全溶解,沉淀是Mg(OH)2,溶液是Na2SO4和NaAlO2混合液,根据守恒有:n(NaOH)=2n(Na2SO4)+n(NaAlO2)=2n(H2SO4)+n(Al)=2×0.1L×2mol/L×+0.08mol=0.48mol,所以c=$\frac{0.48mol}{1mol/L}$=0.48L=480mL,
故答案为:0.02;0.08;480;
(3)当溶液中Mg2+、Al3+恰好沉淀完全时,此时溶液是Na2SO4溶液,根据SO42-离子和Na+离子守恒有:n(Na+)=2n(Na2SO4)=2(H2SO4)=2×0.1L×2mol/L=0.3mol,所以,V(NaOH)=$\frac{0.4mol}{1mol/L}$=0.4L=400mL,
故答案为:400.
点评 本题以图象形式考查混合物计算,难度中等,清楚每一段图象发生的化学反应、知道拐点代表的含义及溶液中溶质的成分,结合方程式对有关问题进行分析,注意运用守恒思想使计算简化.

| A. | HCl | B. | CH3COO- | C. | SO42- | D. | Fe3+ |
| A. | Cu2+、Cl-、H+、SO42- | B. | H+、NO3-、Ba2+、Cl- | ||
| C. | K+、Cl-、H+、SO42- | D. | Ca2+、Na+、Cl-、OH- |
| A. | 氯水应保存在棕色瓶中,久置的氯水,pH值减小 | |
| B. | 新制饱和氯水中存在4个平衡 | |
| C. | 在一定浓度的氯水中加小苏打,$\frac{c(HClO)}{c(C{l}^{-})}$不变 | |
| D. | 饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
| A. | CaCO3与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| B. | 铁与硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化铜与盐酸反应:H++OH-═H2O | |
| D. | 锌与硫酸铜溶液反应:Zn+Cu2+═Zn2++Cu |
| A. | O2 | B. | CO | C. | N2 | D. | CO2 |
 .
. (1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)
(1)由于SiH4具有易提纯的特点,因此硅烷热分解法是制备高纯硅很有发展潜力的方法.制备硅烷整个过程必须严格控制无水,否则生成的硅烷将发生变质,其化学方程式为SiH4+3H2O=4H2+H2SiO3,整个系统还必须与氧隔绝,其原因是SiH4+O2=SiO2+2H2O(用化学方程式表示)