题目内容
【题目】已知: +4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。
+4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O。可用下述装置制取1,2-二溴乙烷(无色液体,密度2.18g·cm-3,熔、沸点为9.79℃、131.4℃,不溶于水);试管d中装有适量液溴(表面覆盖少量水)。

(1)e装置的作用是_______________;当观察到______________________________现象时,试管d中反应基本结束。
(2)若用冰水代替烧杯中的冷水,可能引起的不安全后果是_________________________。
(3)实验结束后精制试管d中粗产品,操作先后顺序是___________________。
A.蒸馏 B.水洗 C.用干燥剂干燥 D.10%NaOH溶液洗
(4)实验消耗40%乙烯利溶液50g,制得产品mg,则乙烯利合成1,2-二溴乙烷的产率为________________(列出含m的计算式即可)。
【答案】吸收溴蒸汽 试管内溶液褪为无色 d中长导管堵塞 DBCA ![]()
【解析】
乙烯利与过量NaOH溶液混合,发生反应![]() +4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O,生成的乙烯进入安全瓶b中,在试管d中乙烯与Br2发生加成反应生成1,2—二溴乙烷,并冷却为液体,为防其凝固,d中温度应控制在1,2—二溴乙烷的熔点以上,这也是设置b装置的目的所在,在e装置中,NaOH吸收d中挥发出的Br2蒸气。
+4NaOH→CH2=CH2↑+NaCl+Na3PO4+3H2O,生成的乙烯进入安全瓶b中,在试管d中乙烯与Br2发生加成反应生成1,2—二溴乙烷,并冷却为液体,为防其凝固,d中温度应控制在1,2—二溴乙烷的熔点以上,这也是设置b装置的目的所在,在e装置中,NaOH吸收d中挥发出的Br2蒸气。
(1)由以上分析知,e装置的作用是吸收d中挥发出的溴蒸汽;水封下的液溴呈深红棕色,与乙烯反应生成的1,2—二溴乙烷呈无色,当Br2完全反应后,混合物呈无色,所以当观察到试管内溶液褪为无色时,试管d中反应基本结束。答案为:吸收溴蒸汽;试管内溶液褪为无色;
(2)若用冰水代替烧杯中的冷水,结合题给1,2—二溴乙烷的熔点,d内生成的1,2—二溴乙烷冷凝为固体,会堵塞导气管,所以可能引起的不安全后果是d中长导管堵塞。答案为:d中长导管堵塞;
(3)实验结束后精制试管d中粗产品时,应先用NaOH溶液除去Br2,再水洗除去溶解在1,2—二溴乙烷中的少量10%NaOH溶液,再去除少量的水,最后进行蒸馏提纯,从而得出操作先后顺序是DBCA。答案为:DBCA;
(4)根据方程式可得关系式![]() ~CH2=CH2~BrCH2CH2Br,则消耗40%乙烯利溶液50g,理论上可生成BrCH2CH2Br的质量为
~CH2=CH2~BrCH2CH2Br,则消耗40%乙烯利溶液50g,理论上可生成BrCH2CH2Br的质量为![]() =
=![]() g,则乙烯利合成1,2—二溴乙烷的产率为
g,则乙烯利合成1,2—二溴乙烷的产率为 =
=![]() 。答案为:
。答案为:![]() 。
。

 阅读快车系列答案
阅读快车系列答案【题目】为探究Na与CO2反应的产物,某化学兴趣小组按如图所示装置进行实验。
己知:CO+2Ag(NH3)2OH=2Ag↓+ (NH4)2CO3+2NH3
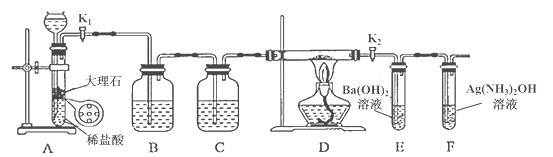
回答下列问题:
(1)B中的溶液为______________。
(2)先称量硬质玻璃管的质量为ml g,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2 g。再进行下列实验操作,其正确顺序是____________(填标号);重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.称量硬质玻璃管
d.打开K1和K2,通入CO2至E中出现浑浊 e.关闭K1和K2 f.冷却到室温
(3)加热硬质玻璃管一段时间,观察到以下现象:
①钠块表面变暗,熔融成金属小球;
②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;
③F中试管内壁有银白物质产生。
产生上述②现象的原因是____________________________________________________;
(4)探究固体产物中钠元素的存在形式
假设一:只有Na2CO3; 假设二:只有Na2O; 假设三:Na2O和Na2CO3均有;
完成下列实验设计,验证上述假设:
步骤 | 操作和现象 | 结论 |
1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
2 | 往步骤1所得滤液中_________________________________; 现象:____________________________________。 |
(5)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式_____________。
m1 | m2 | m3 |
66.7g | 69.0g | 72.1g |