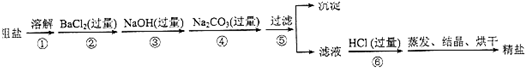
题目内容
10.实验桌上的8杯等物质的量浓度、等体积的溶液,若两两相互混合,则哪一組溶液所含的离子数量最多( )| A. | NaOH+CH3COOH | B. | BaCl2+CuSO4 | C. | AgNO3+NaCl | D. | Na2SO4+NaOH |
分析 假设物质的量都为1mol,考虑电解质的电离以及复分解反应,混合后离子数量最大,则应没有沉淀、气体或弱电解质生成,以此解答该题.
解答 解:假设都为1mol,
A.反应生成CH3COONa,由于CH3COO-水解,则溶液所含的离子数量少于2mol;
B.反应生成硫酸钡沉淀,反应后离子数量为3mol;
C.反应生成AgCl沉淀,反应后离子数量为2mol;
D.不发生反应,离子数量为5mol,
故段D.
点评 本题考查离子反应,为高频考点,侧重考查学生的分析能力,题目难度不大,注意把握常见物质的性质以及离子反应.

练习册系列答案
相关题目
2. 在一定条件下,向一带活塞的密闭容器中充入2mol A和1mol B,发生下列反应:
在一定条件下,向一带活塞的密闭容器中充入2mol A和1mol B,发生下列反应:
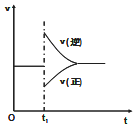
2A(g)+B(g)?2C(g)△H<0.达到平衡后,在t1时刻改变条件,化学反应速率随时间变化如图.下列对t1时刻改变条件的推测中正确的是( )
 在一定条件下,向一带活塞的密闭容器中充入2mol A和1mol B,发生下列反应:
在一定条件下,向一带活塞的密闭容器中充入2mol A和1mol B,发生下列反应:2A(g)+B(g)?2C(g)△H<0.达到平衡后,在t1时刻改变条件,化学反应速率随时间变化如图.下列对t1时刻改变条件的推测中正确的是( )
| A. | 保持压强不变,升高反应温度 | |
| B. | 保持温度不变,增大容器体积 | |
| C. | 保持温度和容器体积不变,充入1 mol C(g) | |
| D. | 保持温度和压强不变,充入1 mol C(g) |
18.下列实验设计和结论相符的是( )
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 | |
| C. | 某无色溶液加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- | |
| D. | 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中溶液变浑浊,一定有CO32- |
5.下列说法中正确的是( )
| A. | 由同种分子构成的物质一定是纯净物 | |
| B. | 纯净物一定由分子构成 | |
| C. | 混合物肯定是由两种以上的元素组成的 | |
| D. | 含有氧元素的化合物就是氧化物 |
15.下列溶液中所含微粒种类最多的是( )
| A. | Na2HPO4溶液 | B. | NH4Cl溶液 | C. | CH3COONa溶液 | D. | NaHCO3溶液 |
2.已知:相同温度下Ka(HF)>Ka(HCN).现有物质的量浓度和体积均相同的NaF和NaCN两种溶液,已知前者溶液中所含离子数目为n1,后者溶液中所含离子数目为n2,下列关系正确的是( )
| A. | 溶液pH:NaF>NaCN | B. | n1>n2 | ||
| C. | H2O的电离程度:NaF>NaCN | D. | c(F-)<c(CN-) |
19.下列实验方法正确的是( )
| A. | 用加热、蒸发的方法除去粗盐中的CaCl2、MgCl2等杂质 | |
| B. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| C. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| D. | 用丁达尔现象区分溶液与胶体 |
1.某课外小组设计的实验室制取乙酸乙酯的装置如图1所示,A中放有浓硫酸,B中放有乙醇(含18O)、无水醋酸钠,D中放有含有酚酞饱和碳酸钠溶液
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
请回答:
(1)浓硫酸的作用是制乙酸、催化剂、吸水剂并作催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3COOH+CH3CH218OH$?_{△}^{浓硫酸}$CH3CO18OC2H5+H2O
(2)球形干燥管C的作用是冷凝和防止倒吸、冷凝.反应结束后D中的现象是液体分层,溶液分层,上层无色油体液体,下层溶液颜色变浅
(3)上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇,减少乙酸乙酯的溶解
(4)欲从D中得到乙酸乙酯的分离方法是分液;从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入生石灰,并用蒸馏法分离出乙醇,再用法除去乙醚,而得到纯净的乙酸乙酯
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹,加热装置已略去),与上如图装置相比,此装置的主要优点有(填写处两点)①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生,②增加了冷凝装置,有利于收集产物乙酸乙酯
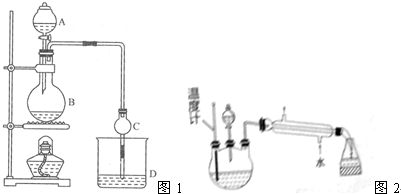
已知①无水氯化钙可与乙醇形成难溶于水的CaCl2•6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
(1)浓硫酸的作用是制乙酸、催化剂、吸水剂并作催化剂、脱水剂;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:CH3COOH+CH3CH218OH$?_{△}^{浓硫酸}$CH3CO18OC2H5+H2O
(2)球形干燥管C的作用是冷凝和防止倒吸、冷凝.反应结束后D中的现象是液体分层,溶液分层,上层无色油体液体,下层溶液颜色变浅
(3)上述实验中饱和碳酸钠溶液的作用是中和乙酸并吸收乙醇,减少乙酸乙酯的溶解
(4)欲从D中得到乙酸乙酯的分离方法是分液;从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入生石灰,并用蒸馏法分离出乙醇,再用法除去乙醚,而得到纯净的乙酸乙酯
(5)某化学课外小组设计了如图2所示的制取乙酸乙酯的装置(图中的铁架台、铁夹,加热装置已略去),与上如图装置相比,此装置的主要优点有(填写处两点)①增加了温度计,便于控制发生装置中反应液的温度,减少副产物的发生,②增加了冷凝装置,有利于收集产物乙酸乙酯