题目内容
11.将含有0.1mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色,下列说法不正确的是( )| A. | 所得红棕色液体为氢氧化铁胶体 | |
| B. | 向该液体中逐滴加盐酸,开始时产生沉淀,盐酸足量时,沉淀消失 | |
| C. | 该液体含分散质微粒0.1 mol | |
| D. | 该液体具有丁达尔现象 |
分析 A.氢氧化铁胶体的制备是在沸水中滴加饱和氯化铁溶液加热到红褐色液体得到氢氧化铁胶体;
B.氢氧化铁胶体遇到电解质溶液会发生聚沉,氢氧化铁程度会溶解在盐酸中;
C.胶体粒子是大量氢氧化铁的聚集体;
D.胶体具有丁达尔效应.
解答 解:A.实验室制备氢氧化铁胶体的方法是在沸水中滴加饱和氯化铁溶液加热,得到红褐色液体为氢氧化铁胶体,故A正确;
B.将含有0.1mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色,向该液体中逐滴加盐酸,开始时胶体聚沉产生沉淀,盐酸足量时,沉淀消失,故B正确;
C.胶体粒子是大量氢氧化铁的聚集体,所以含0.1mol FeCl3溶质的溶液形成胶体后,胶体粒子小于0.1mol,故C错误;
D.将含有0.1mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色为氢氧化铁胶体,具有丁达尔现象,故D正确;
故选A.
点评 本题考查了分散系溶液、浊液、胶体的区别,胶体的性质及鉴别等,注意相关基础知识的积累,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.下列叙述正确的是( )
| A. | 稀硝酸是弱酸,浓硝酸是强酸 | |
| B. | 稀硝酸与活泼金属反应主要放出氢气,而浓硝酸则通常使金属钝化 | |
| C. | 浓硝酸、稀硝酸和浓硫酸都是强氧化剂 | |
| D. | 室温下,铜既可与浓硝酸反应,又可与稀硫酸反应 |
20.某原电池结构如图所示,下列有关该原电池的说法错误的是( )
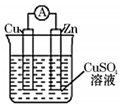

| A. | 锌棒为负极 | B. | 锌棒发生氧化反应 | ||
| C. | 反应后铜棒质量增重 | D. | 电子从铜棒经外电路流向锌棒 |
6.下列叙述正确的是( )
| A. | 向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 | |
| B. | 分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 | |
| C. | Fe(OH)3胶体的电泳现象证明此胶体带正电荷 | |
| D. | 胶体区别于其他分散系的根本原因是胶体有丁达尔效应 |
16.下列关于氯水的叙述错误的是( )
| A. | 新制氯水中只含Cl2和H2O分子 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 光照氯水有气泡放出,该气体是O2 | |
| D. | 氯水放置数天后酸性增强 |
20.下列有关金属腐蚀与防护的说法不正确的是( )
| A. | 纯银器的表面在空气中因化学腐蚀渐渐变暗 | |
| B. | 当镀锡铁制品的镀层破损时,镀层不能对铁制品起保护作用 | |
| C. | 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 | |
| D. | 可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
 .
.