题目内容
20.某原电池结构如图所示,下列有关该原电池的说法错误的是( )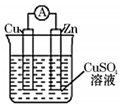
| A. | 锌棒为负极 | B. | 锌棒发生氧化反应 | ||
| C. | 反应后铜棒质量增重 | D. | 电子从铜棒经外电路流向锌棒 |
分析 该装置中,锌易失电子发生氧化反应而作负极,铜作正极,正极上铜离子得电子发生还原反应,电子从负极沿导线流向正极,据此分析解答.
解答 解:A.该装置中,锌易失电子发生氧化反应而作负极,故A正确;
B.该装置中,锌作负极失电子发生氧化反应,故B正确;
C.铜作正极,正极上铜离子得电子发生还原反应析出铜,导致铜棒质量增重,故C正确;
D.锌作负极,铜作正极,电子从负极锌沿外电路流向正极铜,故D错误;
故选D.
点评 本题考查了原电池原理,根据得失电子的难易程度确定正负极,再结合电子移动方向来分析解答,题目难度不大.

练习册系列答案
相关题目
10.下列关于液氯和氯水的叙述中,正确的是( )
| A. | 液氯有酸性,氯水也有酸性 | |
| B. | 液氯和氯水都有漂白性 | |
| C. | 液氯是纯净物,而氯水是混合物 | |
| D. | 液氯无色,氯水呈黄绿色,两者均存在氯离子 |
11.下列离子方程式中,属于水解反应的是( )
| A. | HS-+H2O?H3O++S2- | B. | CO2+2 H2O?HCO3-+H3O+ | ||
| C. | NH4++2H2O?NH3•H2O+H3O+ | D. | HCO3-+OH-?CO32-+H2O |
8.下列化学用语表示正确的是( )
| A. | 碳酸的电离方程式:H2CO3?2H++CO32- | |
| B. | 碱性氢氧燃料电池负极的电极反应式:H2-2e-=2H+ | |
| C. | HCO3-的水解方程式:HCO3-+H2O?CO32-+H3O+ | |
| D. | 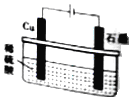 如图所示,反应开始时的离子方程式:Cu+2H+$\frac{\underline{\;通电\;}}{\;}$Cu2++H2↑ |
15.氯元素在自然界的主要存在形式是( )
| A. | Cl2 | B. | HCl | C. | NaCl | D. | KClO3 |
4.化学与社会、生活密切相关.对下列现象或事实的解释正确的是( )
| A. | 过氧化钠用于呼吸面具中是因为过氧化钠是强氧化剂能氧化CO2和水 | |
| B. | FeCl3溶液可用于铜质印刷线路板制作是因为FeCl3能与铜单质发生置换反应 | |
| C. | Al2O3作耐火材料是因为氧化铝熔点高 | |
| D. | 用热的纯碱溶液洗去油污原理是NaHCO3溶液水解显碱性 |
11.将含有0.1mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色,下列说法不正确的是( )
| A. | 所得红棕色液体为氢氧化铁胶体 | |
| B. | 向该液体中逐滴加盐酸,开始时产生沉淀,盐酸足量时,沉淀消失 | |
| C. | 该液体含分散质微粒0.1 mol | |
| D. | 该液体具有丁达尔现象 |
9.在生产和生活中应用的化学知识正确的是( )
| A. | 玻璃、水泥、水晶项链都是硅酸盐制品 | |
| B. | 晶体硅是在通信工程中制作光导纤维的主要原料 | |
| C. | 碳酸钠在医疗上是治疗胃酸过多的一种药剂 | |
| D. | 发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔 |
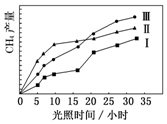 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.