题目内容
3.鉴别KCl溶液和KNO3的试剂是硝酸银溶液,离子方程式为Ag++Cl-=AgCl↓.分析 鉴别KCl溶液和KNO3,可加入硝酸银,生成沉淀的为KCl,以此解答该题.
解答 解:鉴别KCl溶液和KNO3,可加入硝酸银,生成沉淀的为KCl,反应的离子方程式为Ag++Cl-=AgCl↓,故答案为:硝酸银溶液;Ag++Cl-=AgCl↓.
点评 本题考查物质的检验和鉴别,为高频考点,侧重考查学生的分析、实验能力,难度不大,注意把握物质的性质的异同.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
14.室温下进行的下列实验,不能达到预期目的是( )
| 序号 | 实验内容 | 实验目的 |
| A. | 用pH试纸测定相同浓度的CH3COONa溶液和NaHCO3溶液的pH | 比较CH3COOH和H2CO3的酸性强弱 |
| B. | 向AgCl浊液中滴加少量的0.1mol•L-1Na2S溶液 | 比较AgCl和Ag2S的溶度积大小 |
| C. | 向1 mol•L-1的稀硫酸中加入ag锌粉,向4 mol•L-1的稀硫酸的中加入ag锌粒 | 探究固体表面积对Zn与稀硫酸反应速率的影响 |
| D. | 将两个完全相同且充满NO2气体的密闭烧瓶分别浸在热水和冰水中 | 探究温度对化学平衡的影响 |
| A. | A | B. | B | C. | C | D. | D |
15.氯元素在自然界的主要存在形式是( )
| A. | Cl2 | B. | HCl | C. | NaCl | D. | KClO3 |
11.将含有0.1mol氯化铁的饱和溶液逐滴加入到沸水中,并继续加热至溶液呈红棕色,下列说法不正确的是( )
| A. | 所得红棕色液体为氢氧化铁胶体 | |
| B. | 向该液体中逐滴加盐酸,开始时产生沉淀,盐酸足量时,沉淀消失 | |
| C. | 该液体含分散质微粒0.1 mol | |
| D. | 该液体具有丁达尔现象 |
18.手指上有油脂(有机物)、氯化钠、水等分泌物,将按有指纹的白纸置于盛有少量单质碘的烧杯上,微热,即可显现出棕色指纹.下列碘的性质与该实验无关的是( )
| A. | 易升华 | B. | 蒸气呈紫色 | C. | 易溶于油脂 | D. | 与淀粉显蓝色 |
15.从矿物学资料查得,一定条件下自然界存在如下反应:14CuSO4+5FeS2+12H2O→7Cu2S+5FeSO4+12H2SO4.下列说法正确的是( )
| A. | Cu2S既是氧化产物又是还原产物 | |
| B. | 发生反应,有10mol电子转移 | |
| C. | 产物中的SO42-有一部分是氧化产物 | |
| D. | FeS2既是氧化剂又是还原剂 |
12.下列说法错误的是( )
| A. | Na2SO3与BaCl2溶液作用,有白色沉淀生成,加稀HNO3后沉淀消失 | |
| B. | 将SO2气体分别通入Ba(OH)2溶液、FeCl3与BaCl2的混合溶液、HNO3酸化的BaCl2溶液中,均可有白色沉淀生成 | |
| C. | 将SO2气体通入BaCl2溶液中没有白色沉淀生成,将SO2气体通入Ba(NO3)2溶液中有白色沉淀生成 | |
| D. | 将SO2气体、Cl2一起通入BaCl2溶液中,或将SO2气体、NO2气体一起通入BaCl2 溶液中,均有白色沉淀生成 |
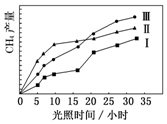 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.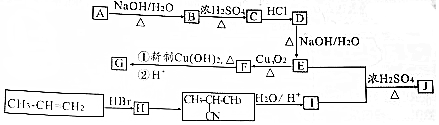
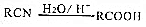
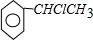 +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$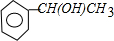 +NaCl;
+NaCl;