题目内容
4.下列离子方程式正确的是( )| A. | 向NaHSO4溶液中滴加Ba(OH)2溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| B. | 向饱和Na2CO3溶液中通入足量CO2:2Na++CO32-+CO2+H2O=2NaHCO3↓ | |
| C. | 向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液:Ca2++HCO3-+2OH-=CaCO3↓+CO32-+2H2O | |
| D. | 硫酸溶液于氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
分析 A.溶液显示中性,硫酸氢钠与氢氧化钡按照物质的量2:1进行反应,据此写出反应的离子方程式;
B.反应生成碳酸氢钠,饱和溶液析出晶体;
C.向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液,碳酸氢钙和氢氧化钙全部反应生成碳酸钙和水;
D.氢氧化钡与稀硫酸1:1反应生成硫酸钡沉淀和水.
解答 解:A.溶液恰好为中性,必须满足氢离子与氢氧根离子的物质的量相等,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.反应生成碳酸氢钠,饱和溶液析出晶体,离子反应为2Na++CO32-+CO2+H2O=2NaHCO3↓,故B正确;
C.向Ca(HCO3)2溶液中加入足量Ca(OH)2溶液,碳酸氢钙和氢氧化钙全部反应生成碳酸钙和水,反应的离子方程式为:Ca2++HCO3-+OH-=CaCO3↓+H2O,故C错误;
D.氢氧化钡与稀硫酸1:1反应生成硫酸钡沉淀和水,离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式书写方法、离子方程式正误判断,注意反应物量不同产物不同,题目难度中等.

练习册系列答案
相关题目
14.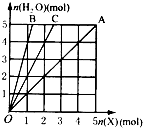 如图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是( )
如图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是( )
 如图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是( )
如图所示,横坐标表示完全燃烧时消耗可燃气体X(X=A、B、C)的物质的量n(X),纵坐标表示燃烧时生成水的物质的量n(H2O),A、B是两种可燃气体,C是A和B的混合气体,则C的成分及体积比可能是( )| A. | C2H4与C3H4,体积比为任意比 | B. | H2与C4H8,体积比2:1 | ||
| C. | C2H2与C3H8,体积比1:2 | D. | H2与C2H6,体积比3:1 |
12. 第三十届奥林匹克夏季运动会将于2012年7月27日在伦敦举行.下图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃.下列说法不正确的是( )
第三十届奥林匹克夏季运动会将于2012年7月27日在伦敦举行.下图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃.下列说法不正确的是( )
 第三十届奥林匹克夏季运动会将于2012年7月27日在伦敦举行.下图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃.下列说法不正确的是( )
第三十届奥林匹克夏季运动会将于2012年7月27日在伦敦举行.下图是酷似奥林匹克旗中五环的一种有机物,被称之为奥林匹克烃.下列说法不正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 该有机物的分子式为C22H14 | |
| C. | 该有机物的一氯代物有7种 | |
| D. | 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
8.下列各组离子中,在酸性溶液中能够大量共存,且通入Cl2后没有明显变化的是( )
| A. | K+、Na+、Cl-、I- | B. | Ca2+、Mg2+、HCO3-、NO3- | ||
| C. | K+、Cu2+、SO42-、Cl- | D. | Ag+、Ba2+、NO3-、CO32- |
6.下列反应的离子方程式正确的是( )
| A. | .碳酸氢钙溶液中加入氢氧化钠溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 用胃舒平治疗胃酸过多:Al(OH)3+3H+═Al3++3H2O | |
| C. | Na与H2O反应:Na+2H2O═Na++2OH-+H2↑ | |
| D. | 碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
 ;U元素在周期表中的位置是第二周期IVA族.
;U元素在周期表中的位置是第二周期IVA族.
 .
.