题目内容
4.某强酸性无色透明溶液中,可大量共存的离子组是( )| A. | Na+、HCO3-、SO42-、Br- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Na+、Cu2+、SO42-、NO3- | D. | Na+、Ba2+、Cl-、SO42- |
分析 强酸性溶液中存在大量氢离子,无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,
A.碳酸氢根离子与氢离子反应;
B.四种离子之间不反应,都不与氢离子反应,且为无色溶液;
C.铜离子为有色离子,不满足溶液无色的条件;
D.钡离子与硫酸根离子反应生成硫酸钡沉淀.
解答 解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,强酸性溶液中存在大量氢离子,
A.HCO3-与强酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.Mg2+、Na+、SO42-、Cl-之间不发生反应,都是无色离子,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.Cu2+为有色离子,在溶液中不能大量存在,故C错误;
D.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,题目难度不大,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
15.下列描述正确的是( )
| A. | 向浓氨水中滴加饱和FeCl3溶液,可以制得Fe(OH)3胶体 | |
| B. | 为除去Mg(OH)2固体中少量Ca(OH)2,可用饱和MgCl2溶液多次洗涤后,再水洗、干燥 | |
| C. | 向溶液X中加入足量盐酸,产生无色无味气体,将气体通入澄清石灰水,产生白色沉淀,说明溶液X中含有CO32- | |
| D. | 验证炭与浓硫酸反应产生的CO2,将炭与浓硫酸反应生成的气体通入盛有澄清石灰水的试管中,观察是否有白色沉淀生成 |
19.下列物质中不能使溴水褪色的是( )
| A. | 甲苯 | B. | 苯乙烯 | C. | 丙炔 | D. | 乙醛 |
16.下列不能证明一元酸HA为弱酸的是( )
| A. | NaA溶液的pH>7(室温下) | |
| B. | pH试纸显示0.1 mol/L HA溶液的pH为2~3(室温下) | |
| C. | 0.1 mol/L的HCl和HA溶液,前者的导电能力明显更强 | |
| D. | HA溶液能与CH3COONa溶液反应生成CH3COOH |
13.下列各元素的氧化物中,既能与盐酸反应生成盐和水,又能够与 NaOH 溶液反应生成盐和水的是( )
| A. | 元素X:它的原子中 M 层比L 层少 2 个电子 | |
| B. | 元素Y:它的焰色反应颜色呈紫色 | |
| C. | 元素Z:它的二价阳离子核外电子总数与氩原子相同 | |
| D. | 元素W:位于元素周期表中的第三周期,ⅢA 族 |
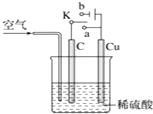 铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题:
铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应.请回答下列问题: