题目内容
13.下列各元素的氧化物中,既能与盐酸反应生成盐和水,又能够与 NaOH 溶液反应生成盐和水的是( )| A. | 元素X:它的原子中 M 层比L 层少 2 个电子 | |
| B. | 元素Y:它的焰色反应颜色呈紫色 | |
| C. | 元素Z:它的二价阳离子核外电子总数与氩原子相同 | |
| D. | 元素W:位于元素周期表中的第三周期,ⅢA 族 |
分析 两性氧化物既能与强酸又能与强碱溶液反应,某种氧化物既能与盐酸反应生成盐和水,又能够与 NaOH 溶液反应生成盐和水,说明该氧化物是两性氧化物,据此分析解答.
解答 解:两性氧化物既能与强酸又能与强碱溶液反应,某种氧化物既能与盐酸反应生成盐和水,又能够与 NaOH 溶液反应生成盐和水,说明该氧化物是两性氧化物,
A.元素X:它的原子中 M 层比L 层少 2 个电子,则X是S元素,二氧化硫或三氧化硫都是酸性氧化物,只能与NaOH反应,不能与稀盐酸反应,故A错误;
B.元素Y:它的焰色反应颜色呈紫色,则Y是K元素,其氧化物是碱性氧化物,只能与稀盐酸反应但不能和NaOH溶液反应,故B错误;
C.元素Z:它的二价阳离子核外电子总数与氩原子相同,则Z是Ca元素,其氧化物是碱性氧化物,只能与稀盐酸反应但不能和NaOH溶液反应,故C错误;
D.元素W:位于元素周期表中的第三周期,ⅢA 族,为Al元素,其氧化物氧化铝是两性氧化物,能与稀盐酸、NaOH溶液反应生成盐和水,故D正确;
故选D.
点评 本题考查原子结构和元素性质关系,为高频考点,侧重考查学生判断及对元素化合物性质的掌握,明确原子结构、元素周期表结构、元素化合物性质是解本题关键,注意基础知识的总结归纳,题目难度不大.

练习册系列答案
相关题目
3.在一定条件下,反应N2+3H2?2NH3,在2L密闭容器中进行,5min内氨的物质的量增加了0.1mol,则反应速率为( )
| A. | v(NH3)=0.03 mol/(L•min) | B. | v(NH3)=0.02 mol/(L•min) | ||
| C. | v(NH3)=0.17 mol/(L•min) | D. | v(NH3)=0.01 mol/(L•min) |
4.某强酸性无色透明溶液中,可大量共存的离子组是( )
| A. | Na+、HCO3-、SO42-、Br- | B. | Mg2+、Na+、SO42-、Cl- | ||
| C. | Na+、Cu2+、SO42-、NO3- | D. | Na+、Ba2+、Cl-、SO42- |
1.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 0.1mol•L-1 稀硫酸中含有SO42-离子个数为0.1NA | |
| B. | 0.1molNa2O2与CO2完全反应,转移电子数为0.2 NA | |
| C. | 常温常压下,46 g的NO2和46g 的N2O4含有的原子数相等 | |
| D. | 标准状况下,22.4L SO3所含的分子数为NA |
2.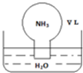 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
 标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )
标准状况下,将体积为VL的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出(无NH3•H2O、NH4+、NH3)扩散到水槽中),所得溶液的密度为ρg•cm-3.下列说法正确的是( )| A. | 条件不足,不能计算所得溶液的物质的量浓度 | |
| B. | 所得溶液中,n(NH3•H2O)+n(NH4+)+n(NH3)=$\frac{V}{22.4}$ | |
| C. | 所得溶液的质量分数为$\frac{17ρ}{22400}$ | |
| D. | 水最终不可能充满整个烧瓶 |
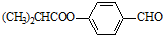 .合成M的一种途径如下:
.合成M的一种途径如下: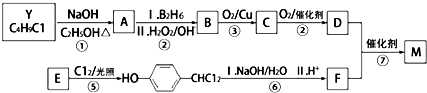
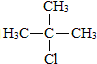 .
. .
.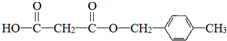 .
.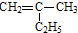 的键线式是
的键线式是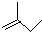
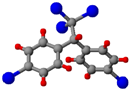 所示.请写出其结构简式
所示.请写出其结构简式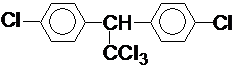
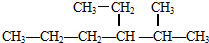 进行命名,它的名称是2-甲基-3-乙基已烷
进行命名,它的名称是2-甲基-3-乙基已烷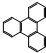 的一氯取代物有2 种.
的一氯取代物有2 种.