题目内容
1.某水溶液中可能存在Na+、Al3+、Fe2+、NH4+、NO3-、CO32-、SO42-中的若干种离子,且各离子的物质的量相同.取该溶液进行如下实验: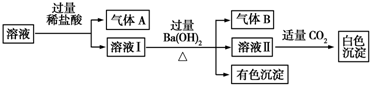
下列判断正确的是( )
| A. | A是CO2,B是NH3 | |
| B. | 白色沉淀一定是Al(OH)3 | |
| C. | 溶液中一定存在Al3+、Fe2+、NO3-、NH4+ | |
| D. | 溶液中一定不存在Na+ |
分析 溶液加入盐酸生成气体,可能含有CO32-,或为Fe2+、NO3-发生氧化还原反应生成NO,溶液Ⅰ加入过量氢氧化钡生成气体B,一定为氨气,则存在NH4+,有色沉淀为氢氧化铁,则含有Fe2+,可知不存在CO32-,存在的各离子具有相同的物质的量,则存在NO3-、SO42-,溶液Ⅱ呈碱性,白色沉淀可能为碳酸钡,以此解答该题.
解答 解:溶液加入盐酸生成气体,可能含有CO32-,或为Fe2+、NO3-发生氧化还原反应生成NO,溶液Ⅰ加入过量氢氧化钡生成气体B,一定为氨气,则存在NH4+,有色沉淀为氢氧化铁,则含有Fe2+,可知不存在CO32-,存在的各离子具有相同的物质的量,则存在NO3-、SO42-,溶液Ⅱ呈碱性,白色沉淀可能为碳酸钡,
A.由以上分析可知A为NO,故A错误;
B.溶液Ⅱ呈碱性,白色沉淀可能为氢氧化铝、碳酸钡等,故B错误;
C.不能确定是否含有Al3+,故C错误;
D.题中存在的各离子具有相同的物质的量,含有Fe2+、NH4+、NO3-、SO42-,不含Na+,故D正确.
故选D.
点评 本题考查了离子共存、常见离子的检验方法,题目难度中等,注意掌握常见离子的性质及检验方法,要求学生能够根据反应现象判断离子存在情况,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
11.下列各组离子在水溶液中能大量共存的是( )
| A. | Na+、SO42-、Cu2+、Cl- | B. | Fe2+、Na+、OH-、K+ | ||
| C. | K+、CO32-、Cl-、Ag+ | D. | H+、Cl-、Na+、CO32- |
16.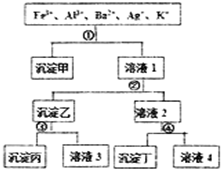 某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3•H2O、NaCl四种溶液,按图所示步骤分开五种离子.下列判断正确的是( )
某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3•H2O、NaCl四种溶液,按图所示步骤分开五种离子.下列判断正确的是( )
 某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3•H2O、NaCl四种溶液,按图所示步骤分开五种离子.下列判断正确的是( )
某溶液含有Fe3+、Al3+、Ba2+、Ag+、K+五种阳离子,现用过量的H2SO4、NaOH、NH3•H2O、NaCl四种溶液,按图所示步骤分开五种离子.下列判断正确的是( )| A. | 沉淀乙是氢氧化铝和氢氧化银的混合物 | |
| B. | 溶液3中含有Al3+ | |
| C. | 试剂①是NaCl,试剂④是H2SO4 | |
| D. | 溶液4含有三种阳离子,分别是H+、Na+、K+ |
6.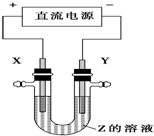 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 在铁片上镀铜时,Y是纯铜 | |
| D. | 外加电流的阴极保护法中,Y是待保护金属 |
10.除去小苏打溶液中少量苏打的方法是( )
| A. | 加热 | B. | 加NaOH | C. | 通CO2气体 | D. | 加盐酸 |
11.苯和甲苯相比较,下列叙述中不正确的是( )
| A. | 都属于芳香烃 | B. | 都能使KMnO4酸性溶液褪色 | ||
| C. | 都能在空气中燃烧 | D. | 都能发生取代反应 |