题目内容
6.相同质量的SO2和SO3它们之间的关系是( )| A. | 所含硫原子的物质的量之比为1:1 | B. | 氧原子的物质的量之比为3:2 | ||
| C. | 氧元素的质量比为2:3 | D. | 硫元素的质量比为5:4 |
分析 已知M(SO2)=64g/mol,M(SO3)=80g/mol,结合n=$\frac{m}{M}$和分子的组成计算.
解答 解:设两种物质的质量都为1g,则SO2和SO3的物质的量之比为$\frac{1g}{64g/mol}$:$\frac{1g}{80g/mol}$=5:4,
A.所含硫原子的物质的量之比等于SO2和SO3的物质的量之比,比值为5:4,故A错误;
B.氧原子的物质的量之比为5×2:4×3=5:6,故B错误;
C.氧元素的质量之比等于氧原子的物质的量之比,为5:6,故C错误;
D.硫元素的质量之比等于硫原子的物质的量之比等于SO2和SO3的物质的量之比,5:4,故D正确.
故选D.
点评 本题考查物质的量的相关计算,为高频考点,侧重学生的分析、计算能力的考查,注意把握物质的构成特点,难度不大.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5 NA | |
| B. | 标准状况下,11.2 L H2O 中含有的分子数目为0.5NA | |
| C. | 0.10 mol Fe 粉与足量水蒸气反应生成的H2分子数为0.10 NA | |
| D. | 25℃,1.01×105Pa,64gSO2中含有的原子数为3 NA |
17.在水中加入下列物质,可使水的电离平衡正向移动的是( )
| A. | NaOH | B. | NH4Cl | C. | NaCl | D. | H2SO4 |
14.向一定质量的稀盐酸中加入镁粉至过量,图中横坐标表示镁粉的质量,则纵坐标表示( ) 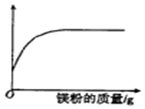

| A. | 溶液的质量 | B. | 稀盐酸的质量 | C. | 氯化镁的质量 | D. | 生成气体的质量 |
1.下列事实不能用勒夏特列原理解释的是( )
| A. | 向氯水中加食盐不利于氯气的溶解 | |
| B. | 棕红色NO2加压后颜色先变深后变浅 | |
| C. | SO2催化氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 高压有利于合成氨的反应 |
11.为证明醋酸是弱电解质,下列方法不正确的是( )
| A. | 测定0.1mol•L-1醋酸溶液的pH | |
| B. | 测定0.1 mol•L-1CH3COONa溶液的酸碱性 | |
| C. | 比较浓度均为0.1 mol•L-1盐酸和醋酸溶液的导电能力 | |
| D. | 比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积 |
18.化学“家庭小实验”是利用家庭日常生活用品进行化学学习和探究的活动.下列利用家庭日常生活用品进行的实验都能达到如期目的一组是( )
①用碘酒来证明马铃薯中含有淀粉
②用食醋除去热水瓶中的水垢
③用肥皂水来检验自来水是否含有过多的Ca2+、Mg2+
④用聚光手电筒检验淀粉溶液具有丁达尔现象
⑤用肥皂水涂抹被蜂、蚁蜇咬后而引起的皮肤肿痛
⑥用食盐来吸收摔破的水银温度计中的水银.
①用碘酒来证明马铃薯中含有淀粉
②用食醋除去热水瓶中的水垢
③用肥皂水来检验自来水是否含有过多的Ca2+、Mg2+
④用聚光手电筒检验淀粉溶液具有丁达尔现象
⑤用肥皂水涂抹被蜂、蚁蜇咬后而引起的皮肤肿痛
⑥用食盐来吸收摔破的水银温度计中的水银.
| A. | ①②⑤⑥ | B. | ①②③④⑤ | C. | ②③④⑥ | D. | ①②③④⑥ |
15.下列离子方程式中正确的是( )
| A. | 工业上粗硅的制备:SiO2+C$\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| B. | Cu2O与稀H2SO4反应:Cu2O+2H+═2Cu++H2O | |
| C. | 用稀硝酸洗涤试管内壁的银镜:3Ag+4H++NO3-═3Ag++NO↑+2H2O | |
| D. | 向Mg(HCO3)2溶液中加足量烧碱溶液:Mg2++2HCO3-+2OH-═MgCO3↓+2H2O+CO32- |
16.在一定温度下的定容密闭容器中,下列说法不能表明反应A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A. | B的物质的量浓度 | B. | 混合气体的压强不变 | ||
| C. | 混合气体的密度 | D. | 混合气体的相对分子质量不变 |