题目内容
20.下列离子方程式正确的是( )| A. | Ca(HCO3)2与少量NaOH溶液的反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| B. | 少量SO2通入NaClO溶液中:3ClO-+SO2+H2O═Cl-+SO42-+2HClO | |
| C. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O | |
| D. | NH4HSO4和少量Ba(OH)2溶液反应NH4++H++SO42-+Ba2++2OH-═BaSO4↓+NH3•H2O+H2O |
分析 A.氢氧化钠少量,生成的碳酸根离子都转化成碳酸钙沉淀;
B.二氧化硫少量,反应生成氯化钠、硫酸钠和次氯酸;
C.草酸为弱酸,离子方程式中草酸不能拆开;
D.氢氧化钡少量,氢氧根离子不足,氢离子优先反应,铵根离子不参与反应.
解答 解:A.Ca(HCO3)2与少量NaOH溶液,反应生成碳酸氢钠、碳酸钙沉淀和水,正确的离子方程式为:Ca2++HCO3-+OH-═CaCO3↓+H2O,故A错误;
B.少量SO2通入NaClO溶液中,二者发生氧化还原反应,反应的离子方程式为:3ClO-+SO2+H2O═Cl-+SO42-+2HClO,故B正确;
C.用高锰酸钾标准溶液滴定草酸,草酸需要保留分子式,正确的离子方程式为:2MnO4-+6H++5H2C2O4═2Mn2++10CO2↑+8H2O,故C错误;
D.NH4HSO4和少量Ba(OH)2溶液,氢离子优先反应,铵根离子不反应,正确的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度不大,注意掌握离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
10.下列烷烃的一氯取代物中没有同分异构体的是( )
| A. | 2-甲基丙烷 | B. | 丙烷 | C. | 丁烷 | D. | 甲烷 |
8.在25℃时,用蒸馏水稀释1mol/L氨水至0.01 mol/L,随溶液的稀释,下列各项中始终保持增大趋势的是( )
| A. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | B. | $\frac{c(N{{H}_{4}}^{+})}{c(O{H}^{-})}$ | ||
| C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$ | D. | c(OH-) |
9.以下反应最符合绿色化学原子经济性(即:原子利用率为100%)要求的是( )
| A. | 甲苯与硝酸制TNT | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 溴乙烷水解制乙醇 | D. | 乙烯聚合为聚乙烯高分子材料 |
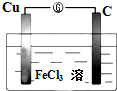 如图所示的原电池中:
如图所示的原电池中: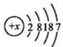
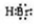 、CaBr2:
、CaBr2: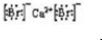 .
.