题目内容
工业上采用乙烯和水蒸气在催化剂(磷酸/硅藻土)表面合成乙醇,反应原理为:CH2=CH2(g)+H2O(g)?CH3CH2OH(g)△H<0,达到平衡时,要使反应速率加快,同时乙烯的转化率提高,应采取的措施是( )
| A、充入氦气 | B、分离除乙醇 |
| C、增大压强 | D、升高温度 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:要使反应速率加快,同时乙烯的转化率提高,方法有升高温度,增大有气体参加的反应的压强等;提高乙烯的转化率,使反应向着正反应方向移动,由此分析解答.
解答:
解:A、充入氦气,体积不变的情况,各组分的浓度不变,反应速率不变,平衡不移动;体积可变充入氦气,相当于减小压强,速率减慢,平衡逆向移动,乙烯的转化率降低,故A错误;
B、分离除乙醇,平衡正向移动,乙烯的转化率提高,但反应速率减小,故B错误;
C、增大压强,反应速率加快,平衡正向移动,乙烯的转化率提高,故C正确;
D、升高温度,反应速率加快,平衡逆向移动,乙烯的转化率降低,故D错误;
故选C.
B、分离除乙醇,平衡正向移动,乙烯的转化率提高,但反应速率减小,故B错误;
C、增大压强,反应速率加快,平衡正向移动,乙烯的转化率提高,故C正确;
D、升高温度,反应速率加快,平衡逆向移动,乙烯的转化率降低,故D错误;
故选C.
点评:本题考查了外界条件对化学平衡及化学反应速率的影响,本题难度中等.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
可逆反应3Fe(s)+4H2O(g)?Fe3O4(g)+4H2(g)在容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A、保持容器体积不变,加入水蒸气 |
| B、将容器的容积缩小一半 |
| C、保持容器容积不变,充入N2使体系压强增大 |
| D、保持压强不变,充入N2使体系容积增大 |
下列物质中,含有自由移动的Cl-的是( )
| A、KCl固体 |
| B、HCl气体 |
| C、KClO3溶液 |
| D、MgCl2溶液 |
下列有关化学用语的表示正确的是( )
A、N2的电子式: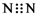 | ||
B、CH4的比例模型: | ||
C、中子数为45的溴原子:
| ||
D、对羟基苯甲酸的结构简式: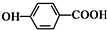 |