题目内容
可逆反应:2A(g)+B(g)?3C(s)+D(g).试根据下图回答:

(1)温度T1℃比 T2℃ (填高、低); 该反应的正反应为 热反应(填吸、放);
(2)甲图纵轴可以表示 (填序号).
①A的转化率 ②B的物质的量 ③C的百分含量 ④混合气体的总质量.

(1)温度T1℃比 T2℃
(2)甲图纵轴可以表示
①A的转化率 ②B的物质的量 ③C的百分含量 ④混合气体的总质量.
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)温度越高,化学反应速率越快,升高温度,化学平衡向着吸热方向进行;
(2)增大压强,化学反应速率加快,化学平衡向着正方向进行,据此回答判断.
(2)增大压强,化学反应速率加快,化学平衡向着正方向进行,据此回答判断.
解答:
解:(1)温度越高,化学反应速率越快,先达到平衡状态,所以T1℃比 T2℃低,升高温度,A的百分含量减小了,即向着正方向进行的,所以该反应的正反应为吸热反应,故答案为:低;吸热;
(2)增大压强,化学反应速率加快,先达到平衡状态,所以P2大于P1,加压,化学平衡向着正方向进行,B的物质的量减小,A的转化率增大,C的百分含量增加,混合气体的总质量减小,②④正确.故答案为:②④.
(2)增大压强,化学反应速率加快,先达到平衡状态,所以P2大于P1,加压,化学平衡向着正方向进行,B的物质的量减小,A的转化率增大,C的百分含量增加,混合气体的总质量减小,②④正确.故答案为:②④.
点评:本题以图象的方式考查学生影响化学平衡移动的因素以及影响化学反应速率的因素,注意知识的迁移和应用是关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
铝条与稀盐酸反应时,下列因素不会影响氢气产生速率的是( )
| A、盐酸的浓度 |
| B、铝条的表面积 |
| C、溶液的温度 |
| D、加少量Na2SO4 |
下列说法正确的是( )
| A、Ca(HCO3)2、Fe(OH)3、FeCl2均可由化合反应制得 |
| B、金属与盐溶液反应都是置换反应 |
| C、液氨、液氯、液态氯化氢都是非电解质 |
| D、凡能电离出氢离子的化合物都是酸 |
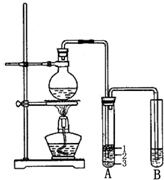 实验室制取少量溴乙烷的装置如图所示.
实验室制取少量溴乙烷的装置如图所示.
