题目内容
下列关于强弱电解质的说法中,正确的是( )
| A、MgO在熔化状态下全部电离,是弱电解质 |
| B、具有极性键的共价化合物都是强电解质 |
| C、具有非极性键的共价化合物都是弱电解质 |
| D、所有弱酸、弱碱都是弱电解质 |
考点:强电解质和弱电解质的概念
专题:电离平衡与溶液的pH专题
分析:A.根据强弱电解质的根本区别在于能够完全电离进行分析;
B.强极性共价化合物是否能在水溶液中完全电离是判断其是否为强电解质的标准;
C.强弱电解质的本质区别是在溶液中能否完全电离,与是否具有非极性键无关;
D.强酸、强碱及大部分盐类在水溶液中或熔融时能完全电离,是强电解质,所有弱酸、弱碱都是弱电解质;
B.强极性共价化合物是否能在水溶液中完全电离是判断其是否为强电解质的标准;
C.强弱电解质的本质区别是在溶液中能否完全电离,与是否具有非极性键无关;
D.强酸、强碱及大部分盐类在水溶液中或熔融时能完全电离,是强电解质,所有弱酸、弱碱都是弱电解质;
解答:
解:A.电解质的强弱是根据其电离程度划分的,完全电离的电解质是强电解质,MgO在熔化状态下全部电离,属于强电解质,故A错误;
B.具有强极性键的共价化合物在水溶液中可能完全电离,如氯化氢属于强电解质,但具有极性键的共价化合物不一定是强电解质,如氟的非金属性最强,HF强极性共价化合物,但HF在水溶液中部分电离,为弱电解质,故B错误;
C.苯磺酸属于强电解质,其碳碳键为非极性键,故C错误;
D.弱酸弱碱在水溶液中部分电离,属于弱电解质,故D正确;
故选D.
B.具有强极性键的共价化合物在水溶液中可能完全电离,如氯化氢属于强电解质,但具有极性键的共价化合物不一定是强电解质,如氟的非金属性最强,HF强极性共价化合物,但HF在水溶液中部分电离,为弱电解质,故B错误;
C.苯磺酸属于强电解质,其碳碳键为非极性键,故C错误;
D.弱酸弱碱在水溶液中部分电离,属于弱电解质,故D正确;
故选D.
点评:本题考查了电解质强弱的判断,注意电解质强弱是根据其电离程度划分,注意明确强弱电解质的本质区别,明确溶液导电性、溶质的溶解度等与强弱电解质没有必然关系是高频考点,题目难度不大.

练习册系列答案
相关题目
已知一定温度和压强下,N2(g)和H2(g)反应生成2molNH3(g),放出92.4kJ热量.在同温同压下向密闭容器中通入1molN2和3molH2,达平衡时放出热量为Q1kJ;向另一体积相同的容器中通入2molN2和3molH2,相同温度下达到平衡时放出热量为Q2kJ.则下列叙述正确的是( )
| A、2Q2>Q1=92.4kJ |
| B、2Q2=Q1=92.4kJ |
| C、Q1<Q2<92.4kJ |
| D、2Q2=Q1<92.4kJ |
下列关于有机化合物的认识正确的是( )
| A、蛋白质在空气中完全燃烧转化为水和二氧化碳 |
| B、淀粉与纤维素的分子式都是(C6H10O5)n,二者互为同分异构体 |
| C、乙烯均可使溴水和高锰酸钾溶液褪色,是因为都发生了加成反应 |
| D、在浓硫酸存在下,乙酸与乙醇共热生成乙酸乙酯的反应为取代反应 |
常温时,下列各组粒子在指定条件下,一定能大量共存的是( )
| A、水电离出c(H+)=10-13mol/L 的溶液中:Fe2+ NO3- k+Cl- |
| B、在NaAlO2溶液中:k+CO32- SO42-S2- |
| C、甲基橙呈红色溶液中:Na+ ClO- Al3+ NO3- |
| D、含FeCl3 溶液中:Cl- k+ H2O2NO3- |
下列叙述不正确的是( )
| A、光照氯水有气泡逸出,该气体是Cl2 |
| B、工业上可用碳在高温下还原二氧化硅制取硅 |
| C、工业上可用氯气和石灰乳为原料制造漂白粉 |
| D、将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路 |
下列有关化学用语表示正确的是( )
| A、氢的三种同位素:H2、D2、T2 |
B、F-的结构示意图: |
| C、中子数为20的氯原子:2017Cl |
D、NH3的电子式: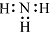 |