��Ŀ����
8����ҵ����ʳ�Ρ�������������̼������Ϊԭ����ȡ�����1��ʵ�����ᴿ���ε�һ����Ҫ�����dz�ȥ����ˮ�е����������ӣ�ij������Ʒ����Ҫ��Ca2+��Mg2+�����ᴿ�ô���ʱ���ɿ����ڴ���ˮ�м��������A��B�����ʣ�������A��Դ��ʯ��Ҥ������д��A��B�Ļ�ѧʽ��
ACa��OH��2��CaO��BNa2CO3��
��2������ʵ���������Ϊ��ȡ�����ܽ⡢���������ˡ����������pH����������ȴ�ᾧ��
��3�����ϡ����������pH��Ŀ���dz�ȥ������NaOH��Na2CO3��
��4��д�ɹ�ҵ����ʳ�Ρ�������������̼������Ϊԭ����ȡ���Ӧ�Ļ�ѧ����ʽ��NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl
2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2��
��2�������������̼ͨ����Ⱥ�˳���ǣ���ͨ��NH3��ͨ��CO2����Ϊ���������ܽ�Ƚϴ��ұ��Ͱ���ˮ�Լ��ԣ��ȱ���ʳ��ˮ���������ն�����̼��
�ù���û������̼���ƾ��壬��ԭ����̼���Ƶ��ܽ�ȱ�̼�����ƴ�
��6����״���£�����11.2��������̼���壬������������Ҫ1mol/L�İ�ˮ���Ϊ500mL��
���� ���ʵ������ʱ��Ҫ��������ʵ��Ŀ�ĺ�ʵ��ԭ������ʵ��İ�ȫ�ԡ���ѧ�Ժͼ�Լ�����ֽ��н�𣮶Ի�ѧʵ�����ݽ��д���ʱ��Ҫע����ĺ����ԣ�
��1����������AԴ��ʯ��Ҥ��˵��������ʯ�һ���ʯ����������
��2������ʵ�����ᴿ���ε�ʵ�����������ɣ�
��3���������pH��Ŀ���dz�ȥ������NaOH��Na2CO3��
��4���������Ȼ�����Һ��Ϻ��������������̼������Ӧ������NaHCO3��NH4Cl��
��5�����ݰ���ˮ�Լ��ԣ��������ն�����̼��NH3��������ˮ����Һ�������ԣ���ͨ��CO2ʹ֮�����ת��ΪHCO3-��
��6����״���£�����11.2��������̼���壬������������Ҫ1mol/L�İ�ˮ����ɸ��ݹ�ϵʽ��CO2��NH3���м��㣮
��� �⣺��1�������к�����������ӡ�̼������ӡ�þ���ӣ����õ��ᴿʳ�εij�����Ϊ����������Һ��̼������Һ��������A��Դ��ʯ��Ҥ��������A���������ƣ�B��̼���ƣ�
�ʴ�Ϊ��Ca��OH��2��CaO��Na2CO3��
��2��ʵ�����ᴿ���ε�ʵ���������Ϊ��ȡ�����ܽ⡢���������ˡ���������ȴ�ᾧ����ɣ�
�ʴ�Ϊ���ܽ⣻���ˣ�������
��3��������м������pH��Ŀ���dz�ȥ������NaOH��Na2CO3��
�ʴ�Ϊ����ȥ������NaOH��Na2CO3��
��4���������Ȼ�����Һ��Ϻ��������������̼������Ӧ������NaHCO3��NH4Cl��NaHCO3�ٷֽ�ΪNa2CO3��H2O��CO2����Ӧ����ʽΪNH3+CO2+NaCl+H2O=NaHCO3+NH4Cl��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ʴ�Ϊ��NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
��5����Ϊ���Ͱ���ˮ�Լ��ԣ��ȱ���ʳ��ˮ���������ն�����̼���������ð��������������У�Ҫ����ʳ��ˮ��ͨ�백�����Ƴɱ��Ͱ���ˮ����������ͨ�������̼�� ̼���Ƶ��ܽ�ȱ�̼�����ƴ�
�ʴ�Ϊ����ͨ��NH3��ͨ��CO2���������ܽ�Ƚϴ��ұ��Ͱ���ˮ�Լ��ԣ��ȱ���ʳ��ˮ���������ն�����̼�� ̼���Ƶ��ܽ�ȱ�̼�����ƴ�
��6����������������Ҫ1mol/L�İ�ˮ���ΪxmL
��ϵʽ��CO2 ��NH3
22.4L 1mol
11.2L 1mol/L��xmL��$\frac{1L}{1000mL}$
x=500mL
�ʴ�Ϊ��500��
���� ���⿼������ᴿ�����ԭ������ȷ���������ӷ�Ӧ����ⷴӦ�ǽ��Ĺؼ���ע����Ӳ��������µ����ʼ��Լ�������˳����Ŀ�Ѷ��еȣ�

 �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д� ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�| A�� | NH4++H2O=NH3•H2O+H+ | B�� | CO32-+H2O?H2CO3-+2OH- | ||
| C�� | HCO3-+H2O=H++CO32- | D�� | CH3COO-+H2O?CH3COOH+OH- |
| A�� | NaHCO3=Na++H++CO32- | B�� | Na2SO4=Na2++SO42- | ||
| C�� | H2SO4=2H++SO42- | D�� | KClO3=K++Cl-+3O2- |
| A�� | 2.24L CO2�к��е�ԭ����Ϊ0.3NA | |
| B�� | ���³�ѹ�£�92g NO2��N2O4��������к��е�ԭ����Ϊ6NA | |
| C�� | 17g-OH��17g OH-�����ĵ�������Ϊ10NA | |
| D�� | ��״���£�2.24 LCCl4���еĹ��ۼ���Ϊ0.4NA |
| A�� | Na+��CO32-��SO42-��H+ | B�� | K+��AlO2-��H+��Cl- | ||
| C�� | Fe2+��K+��H+��SO42- | D�� | A13+��H+��NO3-��SO42- |
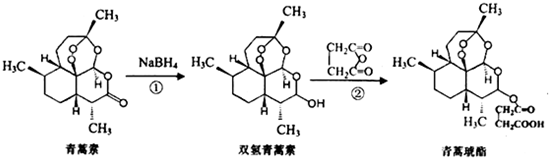
| A�� | �����ط���ʽΪC15H22O5 | |
| B�� | ����������NaOH��Һ��Ӧ | |
| C�� | ��Ӧ��ԭ��������Ϊ100% | |
| D�� | ����������������������Һ��Ӧ���������������� |
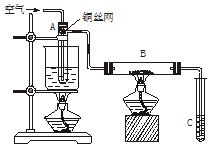 ��ͼ��ʾ�����Ҵ��Ĵ�����ʵ�飬�Թ�A��ʢ����ˮ�Ҵ���B��װ��CuO����ʯ���������壩����ش��������⣺
��ͼ��ʾ�����Ҵ��Ĵ�����ʵ�飬�Թ�A��ʢ����ˮ�Ҵ���B��װ��CuO����ʯ���������壩����ش��������⣺