题目内容
2.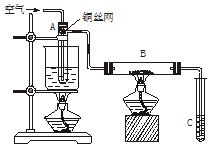 如图所示进行乙醇的催化氧化实验,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体).请回答下列问题:
如图所示进行乙醇的催化氧化实验,试管A中盛有无水乙醇,B中装有CuO(用石棉绒作载体).请回答下列问题:(1)向试管A中鼓入空气的目的是使空气通过乙醇,形成乙醇和空气的混合气体.
(2)试管A上部放置铜丝的作用是防止乙醇和空气的混合气体爆炸.
(3)玻璃管中可观察到的现象是黑色固体变红;相关化学方程式是CuO+C2H5OH$\stackrel{△}{→}$CH3CHO+H2O+Cu,2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
分析 乙醇和氧气在铜作催化剂条件下加热发生氧化还原反应生成乙醛,乙醇在加热条件下也可与氧化铜反应生成乙醛,则A中鼓入空气可提供氧气和乙醇的混合气体,由于乙醛易溶解于水,所以最后出来的气体主要是氮气,以此解答该题.
解答 解:(1)A中通入空气的目的是提供氧化乙醇的氧化剂氧气并形成乙醇和空气的混合气体,
故答案为:使空气通过乙醇,形成乙醇和空气的混合气体;
(2)铜丝在温度较高时可与氧气反应,从而避免乙醇和空气的混合气体爆炸,
故答案为:防止乙醇和空气的混合气体爆炸;
(3)乙醇和氧化铜在加热条件下发生氧化还原反应生成乙醛,反应的方程式为CuO+C2H5OH$\stackrel{△}{→}$CH3CHO+H2O+Cu,同时发生2C2H5OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O,可观察到黑色固体变红,
故答案为:黑色固体变红; CuO+C2H5OH$\stackrel{△}{→}$CH3CHO+H2O+Cu,2C2H5OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O.
点评 本题以乙醇的催化氧化为载体考查学生的分析能力和实验设计能力,为高频考点,注意把握乙醇的性质以及实验的可行性的评价,难度不大.

练习册系列答案
相关题目
7.下列分离或提纯物质的方法正确的是( )
| A. | 用过滤的方法除去NaCl溶液中含有的少量KCl | |
| B. | 用蒸馏的方法制取蒸馏水 | |
| C. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| D. | 用加热、蒸发的方法可以除去CaCl2、MgCl2等杂质 |
10.用下列实验装置和方法进行相应实验,正确的是( )
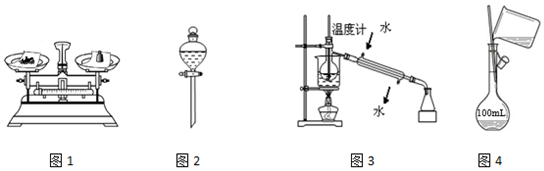

| A. | 用图1所示方法称量固体氯化钠 | |
| B. | 用图2装置分离碘的四氯化碳溶液 | |
| C. | 用图3所示装置和方法进行石油分馏 | |
| D. | 用图4装置配制150 mL稀盐酸 |
7.化学与生活密切相关,下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 食用油反复加热不会产生稠环芳香烃等有害物质 | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 医用消毒酒精中乙醇的浓度为75% |
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.2 mol Na2O2和Na2S的混合物中共含有离子数目为0.6 NA | |
| B. | 1 mol Cl2溶于水的过程中有NA个电子转移 | |
| C. | 常温下,pH=12的氢氧化钠溶液中OH-数目为0.01 NA | |
| D. | 1.0 mol/L FeCl3溶液全部转化成氢氧化铁胶体所得胶粒数目为NA |
11.某无色强酸性溶液中能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、NO3-、SO42-、I- | ||
| C. | Na+、K+、Cl-、S2- | D. | Fe3+、K+、Cl-、SO42- |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2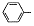 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |