题目内容
5.青蒿琥酯是治疗疟疾的首选药,可由青蒿素两步合成得到.下列有关说法不正确的是( )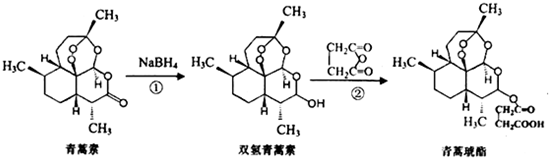
| A. | 青蒿素分子式为C15H22O5 | |
| B. | 青蒿素能与NaOH溶液反应 | |
| C. | 反应②原子利用率为100% | |
| D. | 青蒿琥酯能与氢氧化钠溶液反应可生成青蒿琥酯钠 |
分析 A.根据结构简式确定分子式;
B.青蒿素中含有酯基和醚键,酯基能和NaOH反应;
C.加成反应时原子利用率为100%;
D.青蒿琥酯能与氢氧化钠溶液反应时,酯基水解生成羧酸钠和醇羟基.
解答 解:A.根据结构简式知,其分子式为C15H22O5,故A正确;
B.青蒿素中含有酯基和醚键,酯基能和NaOH发生水解反应,故B正确;
C.反应②为加成反应,原子利用率为100%,故C正确;
D.青蒿琥酯能与氢氧化钠溶液反应时,酯基水解生成羧酸钠和醇羟基,所以得不到青蒿琥酯钠,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,侧重考查羧酸、酯基及加成反应,明确官能团及其性质关系是解本题关键,易错选项是D.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
10.下列实验能获得成功的是( )
①用醋酸钠晶体和碱石灰共热制取甲烷;②将甲烷气体通入溴水中制取溴甲烷;③用酒精灯加热CH4制取炭黑和氢气;④将甲烷气体与溴蒸气混合光照制取纯净的一溴甲烷;⑤用电石和饱和食盐水制取乙炔;⑥用酒精和稀硫酸混合加热至170℃制取乙烯.
①用醋酸钠晶体和碱石灰共热制取甲烷;②将甲烷气体通入溴水中制取溴甲烷;③用酒精灯加热CH4制取炭黑和氢气;④将甲烷气体与溴蒸气混合光照制取纯净的一溴甲烷;⑤用电石和饱和食盐水制取乙炔;⑥用酒精和稀硫酸混合加热至170℃制取乙烯.
| A. | ①②③ | B. | ④⑤⑥ | C. | ⑤ | D. | ④⑥ |
11.设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 1摩尔CH4所含质子数目为10NA | |
| C. | 0.2NA个硫酸分子与19.6g磷酸含有相同的氢原子数 | |
| D. | 18g NH4+所含中子数目为10 NA |
15.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 50℃时,1LpH=1的H2SO4溶液含H+的数目为0.1NA | |
| B. | 1mol锌与浓硫酸完全反应生成SO2和H2的混合气体,气体的分子数小于NA | |
| C. | 100gCaCO3和KHCO3混合固体中的CO32-的数目为NA | |
| D. | 标准状况下,2.24L苯含有的原子数为1.2NA |
10.用下列实验装置和方法进行相应实验,正确的是( )
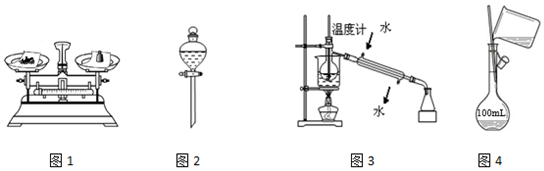

| A. | 用图1所示方法称量固体氯化钠 | |
| B. | 用图2装置分离碘的四氯化碳溶液 | |
| C. | 用图3所示装置和方法进行石油分馏 | |
| D. | 用图4装置配制150 mL稀盐酸 |
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.2 mol Na2O2和Na2S的混合物中共含有离子数目为0.6 NA | |
| B. | 1 mol Cl2溶于水的过程中有NA个电子转移 | |
| C. | 常温下,pH=12的氢氧化钠溶液中OH-数目为0.01 NA | |
| D. | 1.0 mol/L FeCl3溶液全部转化成氢氧化铁胶体所得胶粒数目为NA |
15.如果NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个CO2分子中含1mol氧原子 | |
| B. | 3.2g S2-的核外电子数1.6NA | |
| C. | 1 mol•L-1Na2CO3溶液中含有2NA个Na+ | |
| D. | 1个H2SO4分子中氧原子的质量为64/NAg |