题目内容
3.NA表示阿伏伽德罗常数,下列说法正确的是( )①25℃时,pH=12的1.0LNaClO溶液中水电离出的OH-的数目为0.01NA
②1.0L1.0mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA
③46gNO2和N2O4的混合气体所含氧原子数为2NA
④标准状况下,22.4LCH3Cl含有的分子数为NA
⑤将NA个NH3分子溶于1L水中得到1mol•L-1的氨水
⑥1molSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子.
| A. | ①②③⑥ | B. | ①③ | C. | ②④⑥ | D. | 全部 |
分析 ①25℃时,pH=12的1.0LNaClO溶液中氢氧根全部来自于水的电离;
②1.0L1.0mol•L-1的NaAlO2水溶液中除了偏铝酸钠含有氧原子外,水也含氧原子;
③NO2和N2O4的最简式均为NO2;
④求出CH3Cl的物质的量,然后根据分子个数N=nNA来计算;
⑤将NA个NH3分子溶于1L水中溶液体积大于1L;
⑥SO2与O2的反应为可逆反应.
解答 解:①25℃时,pH=12的1.0LNaClO溶液中氢离子浓度为10-12mol/L,氢氧根浓度为0.01mol/L,而氢氧根全部来自于水的电离,故溶液中水电离出的氢氧根的物质的量为0.01mol,个数为0.01NA个,故①正确;
②1.0L1.0mol•L-1的NaAlO2水溶液中除了偏铝酸钠含有氧原子外,水也含氧原子,故溶液中含有的氧原子的个数大于2NA个,故②错误;
③NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为1mol,故含2NA个氧原子,故③正确;
④标况下22.4LCH3Cl的物质的量为1mol,故分子个数N=nNA=NA个,故④正确;
⑤将NA个NH3分子溶于1L水中溶液体积大于1L,故所得氨水的浓度小于1mol/L,故⑤错误;
⑥SO2与O2的反应为可逆反应,不能进行彻底,故转移的电子数小于2NA个,故⑥错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 0.2 mol Na2O2和Na2S的混合物中共含有离子数目为0.6 NA | |
| B. | 1 mol Cl2溶于水的过程中有NA个电子转移 | |
| C. | 常温下,pH=12的氢氧化钠溶液中OH-数目为0.01 NA | |
| D. | 1.0 mol/L FeCl3溶液全部转化成氢氧化铁胶体所得胶粒数目为NA |
11.某无色强酸性溶液中能大量共存的离子组是( )
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、NO3-、SO42-、I- | ||
| C. | Na+、K+、Cl-、S2- | D. | Fe3+、K+、Cl-、SO42- |
18.在一定条件下,可逆反应X(g)+2Y(g)?2Z (g)△H=-akJ•mol-1,达到化学平衡时,下列说法一定正确的是( )
| A. | 反应放出a kJ热量 | |
| B. | X和Y的物质的量之比为1:2 | |
| C. | 反应物和生成物的浓度都不再发生变化 | |
| D. | X的正反应速率等于Z的逆反应速率 |
8.下列关于钠及其化合物的说法错误的是( )
| A. | 钠着火时可用细砂来灭火 | |
| B. | 切开的金属钠暴露在空气中,光亮的表面变暗发生2Na+O2═Na2O2反应 | |
| C. | 过氧化钠在潮湿空气放一段时间变成白色粘稠物的反应主要是:2Na2O2+2H2O═4NaOH+O2↑ | |
| D. | 过氧化钠投入硫酸铜溶液可产生氢氧化铜沉淀和氧气 |
15.如果NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | NA个CO2分子中含1mol氧原子 | |
| B. | 3.2g S2-的核外电子数1.6NA | |
| C. | 1 mol•L-1Na2CO3溶液中含有2NA个Na+ | |
| D. | 1个H2SO4分子中氧原子的质量为64/NAg |
12.下列表示对应化学反应的离子方程式正确的是( )
| A. | 漂白粉露置在空气中:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用少量氨水吸收二氧化硫:SO2+NH3•H2O=HSO3-+NH4+ | |
| C. | 少量CO2通入苯酚钠溶液:2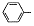 +CO2+H2O→2 +CO2+H2O→2 OH+CO32- OH+CO32- | |
| D. | 磁性氧化铁(Fe3O4)溶于氢碘酸:Fe3O4+8H+═Fe2++2Fe3++4H2O |
16.甲容器进行A→B的反应,△H<0,反应速率为v1,在t1温度下进行;乙容器进行C→D的反应,△H>0,反应速率为v2,在t2温度下进行.对于上述反应,下列说法正确的是( )
| A. | 若t1>t2,则v1>v2 | |
| B. | 甲容器内每分钟减少4mol A,乙容器内每分钟减少2mol C,则甲容器内的反应速率比乙容器内的反应速率快 | |
| C. | 当温度升高时v1增大,v2减小 | |
| D. | 在甲、乙容器中分别加入MnO2,v1、v2不一定加快 |