题目内容
16.如图所示曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,采取的措施不可能是改变了( )
| A. | 温度 | B. | 压强 | C. | 浓度 | D. | 加催化剂 |
分析 由图象可知,由曲线a到曲线b,到达平衡的时间缩短,改变条件,反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,据此结合选项判断.
解答 解:由图象可知,由曲线a到曲线b,到达平衡的时间缩短,改变条件,反应速率加快,且平衡时x的转化率不变,说明条件改变不影响平衡状态的移动,
A、该反应正反应是放热反应,降低温度,反应速率减慢,平衡向正反应移动,x的转化率增大,故A选;
B、气体两边的计量数相等,增大压强,同等程度加大正逆反应速率,但化学平衡不移动,但x的转化率不变,故B不选;
C、同等程度的增加反应物和生成物的浓度,正逆反应速率加快,但化学平衡不移动,但x的转化率不变,故C不选;
D、加入催化剂,反应速率加快,催化剂不影响平衡移动,x的转化率不变,故D不选;
故选A.
点评 本题考查化学平衡移动图象与影响因素,难度中等,根据曲线变化分析条件改变对速率、X转化率的影响是解题的关键.

练习册系列答案
相关题目
6.想一想:Ba(OH)2(固态)、CuSO4(固态)、CH3COOH(液态)这些物质为什么归为一类,下列哪个物质还可以和它们归为一类( )
| A. | 75%的酒精溶液 | B. | 硝酸钠(固态) | C. | Fe(OH)3胶体 | D. | 豆浆 |
4. 在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
 在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )| 选项 | Y的物理意义 | 甲、乙的物理意义 | 甲与乙的大小 |
| A | SO2的转率 | 温度 | 甲>乙 |
| B | SO2的体积分数 | 压强 | 甲>乙 |
| C | SO3的体积分数 | 温度 | 乙>甲 |
| D | SO2的转率 | 压强 | 乙>甲 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
11.分别往含有下列离子的溶液中通入氯气,离子浓度不会减少的是( )
| A. | Ag+ | B. | HCO3- | C. | I- | D. | Na+ |
1.用NA代表阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,2.24LCHCl3的分子数0.1NA | |
| B. | 用惰性电极电解1 L浓度均为2 mol•L-1的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,理论上阴极析出6.35g金属 | |
| C. | 9.2gNO2和N2O4的混合气中含有的氮原子数为大于0.2NA | |
| D. | VL a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
8.有些地区水井中的水刚从井中抽出时是清澈透明的,但烧开后发现产生了红褐色的不溶物.某中学研究性学习小组对这种现象进行了分析:向刚抽出的井水中加入硫氰化钾溶液,无明显现象;向产生不溶物的水中加入盐酸,不溶物溶解,再向其中加入硫氰化钾溶液,溶液呈现血红色.则下列说法不正确的是( )
| A. | 该井水中肯定有Fe3+ | |
| B. | 该井水中肯定有Fe2+ | |
| C. | 红褐色不溶物是Fe(OH)3 | |
| D. | 红褐色不溶物是由于氧化和水解产生 |

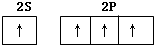
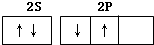

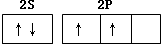
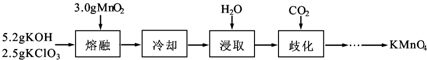
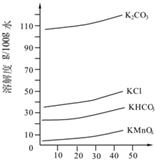 实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下:
实验室用MnO2、KOH及KClO3为原料制取高锰酸钾的实验流程如下: