题目内容
8.有些地区水井中的水刚从井中抽出时是清澈透明的,但烧开后发现产生了红褐色的不溶物.某中学研究性学习小组对这种现象进行了分析:向刚抽出的井水中加入硫氰化钾溶液,无明显现象;向产生不溶物的水中加入盐酸,不溶物溶解,再向其中加入硫氰化钾溶液,溶液呈现血红色.则下列说法不正确的是( )| A. | 该井水中肯定有Fe3+ | |
| B. | 该井水中肯定有Fe2+ | |
| C. | 红褐色不溶物是Fe(OH)3 | |
| D. | 红褐色不溶物是由于氧化和水解产生 |
分析 井中的水刚抽出时清澈透明,烧开后却产生了红褐色的不溶物为氢氧化铁沉淀,向刚抽出的井水中加入硫氰化钾溶液,无明显现象判断井水中一定不含铁离子,推断含有亚铁离子,加热过程中亚铁离子被氧气氧化生成铁离子,铁离子水解生成氢氧化铁沉淀;向产生不溶物的水中加入盐酸,不溶物溶解,再向其中加入硫氰化钾溶液,溶液呈现血红色,证明红褐色沉淀是氢氧化铁.
解答 解:向刚抽出的井水中加入硫氰化钾溶液,无明显现象判断井水中一定不含铁离子,推断含有亚铁离子,加热过程中亚铁离子被氧气氧化生成铁离子,铁离子水解生成氢氧化铁沉淀;向产生不溶物的水中加入盐酸,不溶物溶解,再向其中加入硫氰化钾溶液,溶液呈现血红色,证明红褐色沉淀是氢氧化铁;
A、上述分析可知井水中不含Fe3+,故A错误;
B、依据反应现象分析,井水中含有亚铁离子,故B正确;
C、分析实验现象和沉淀颜色可知,红褐色沉淀为Fe(OH)3,故C正确;
D、红褐色的不溶物为氢氧化铁,受热可以分解生成氧化铁和水,水解生成,亚铁离子发生氧化还原反应,生成铁离子,故D正确;
故选A.
点评 本题考查了铁的化合物性质分析,离子季铵盐方法和实验现象分析判断,掌握基础基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列说法正确的组合是( )
①蔗糖、麦芽糖都是还原性糖
②油脂在NaOH稀溶液中发生皂化反应后,静置不分层,说明水解完全
③淀粉和纤维素都是天然高分子化合物
④蛋白质遇硫酸钠、硫酸铜溶液均会发生变性
⑤用淀粉碘化钾试纸和白醋溶液可以检验加碘盐中的碘
⑥油脂都不能使溴水褪色.
①蔗糖、麦芽糖都是还原性糖
②油脂在NaOH稀溶液中发生皂化反应后,静置不分层,说明水解完全
③淀粉和纤维素都是天然高分子化合物
④蛋白质遇硫酸钠、硫酸铜溶液均会发生变性
⑤用淀粉碘化钾试纸和白醋溶液可以检验加碘盐中的碘
⑥油脂都不能使溴水褪色.
| A. | ①②③ | B. | ④⑤⑥ | C. | ③④⑤ | D. | ②③⑤ |
19.下列叙述错误的是( )
| A. | 金属钠在自然界中可以以单质形式存在 | |
| B. | 金属钠燃烧时发出黄色火焰 | |
| C. | 金属钠保存在煤油中 | |
| D. | 金属钠在空气中燃烧生成过氧化钠 |
16.如图所示曲线a表示放热反应X(g)+Y(g)?Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系.若要改变起始条件,使反应过程按b曲线进行,采取的措施不可能是改变了( )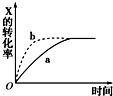

| A. | 温度 | B. | 压强 | C. | 浓度 | D. | 加催化剂 |
3.如图实验装置图能实现对应的实验目的是( )

| A. | 利用图1除去Cl2中的HCl | |
| B. | 利用图2由45°白酒制无水乙醇 | |
| C. | 利用图3检验产物中含有乙烯 | |
| D. | 图4是研究温度对NO2和N2O4平衡的影响 |
13.下列实验误差分析错误的是( )
| A. | 用润湿的pH试纸测稀酸溶液的pH,测定值偏大 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 用标准酸液滴定未知碱液时,若酸式滴定管未润洗,则测定结果偏大 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测结果偏低 |
20.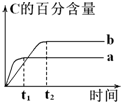 已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
 已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )| A. | a条件下的反应速率小于b条件下的反应速率 | |
| B. | 其他条件相同时,a表示有催化剂,b表示无催化剂 | |
| C. | 其他条件相同,若a、b表示不同压强下的反应,则n>2 | |
| D. | 其他条件相同,若a、b表示不同温度下的反应,则x>0 |
17.下列离子方程式正确的是( )
| A. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H20 | |
| B. | 碳酸钠溶液与少量盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 稀硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO42-═H2O+BaSO4↓ | |
| D. | 氢氧化铜与稀硫酸反应:Cu(OH)2+2H+═Cu2++2H2O |
17.下列说法正确的是( )
| A. | 可以用澄清的石灰水鉴别SO2和CO2 | |
| B. | SO2能使溴水、KMnO4溶液迅速褪色 | |
| C. | 硫粉在过量的氧气中燃烧可得到SO3 | |
| D. | 少量SO2通入到浓的CaCl2溶液能生成白色沉淀 |