题目内容
3.对于某些离子的检验及结论一定正确的是( )| A. | 加入硝酸酸化的硝酸银溶液,有白色沉淀产生,一定有Cl- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润蓝色石蕊试纸变红,一定有NH4+ | |
| D. | 用铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,说明原溶液中一定不含有K+ |
分析 A.白色沉淀为AgCl;
B.白色沉淀可能为AgCl或硫酸钡;
C.检验氨气,利用红色的石蕊试纸;
D.观察K的焰色反应需要透过蓝色的钴玻璃.
解答 解:A.加入硝酸酸化的硝酸银溶液,有白色沉淀产生,白色沉淀为AgCl,则原溶液一定有Cl-,故A正确;
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,沉淀可能为AgCl,则原溶液不一定有SO42-,故B错误;
C.加入氢氧化钠溶液并加热,产生的气体能使湿润色红石蕊试纸变蓝,一定有NH4+,试纸不合理,故C错误;
D.用铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,说明原溶液中一定Na+,不能确定是否含有K+,故D错误;
故选A.
点评 本题考查常见离子的检验方法,为高频考点,把握离子检验的试剂、现象与结论为解答的关键,侧重分析与应用能力的考查,注意检验时排除干扰离子,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
13.下列叙述错误的是( )
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 12g12C 含有约6.02×1023个碳原子 | |
| C. | 在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
14.下列电子式正确的是( )
| A. |  | B. | 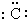 | C. | 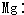 | D. | 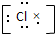 |
11.下列物质能产生丁达尔效应的是( )
| A. | Al(OH)3胶体 | B. | 蒸馏水 | C. | 饱和食盐水 | D. | 纯净的空气 |
18.为纪念俄国化学家门捷列夫,人们把第101号元素(人工合成元素)命名为钔.该元素最稳定的一种原子为 258 Md,关于该原子下列说法正确的是( )
| A. | 质子数是258 | B. | 质量数是101 | C. | 中子数是157 | D. | 电子数是359 |
15.分类法是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
①Fe2O3、CaO、Al2O3都是碱性氧化物
②根据反应中是否有氧气参加,将化学反应分为氧化还原反应和非氧化还原反应
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
④根据纯净物中是否含氧元素,来判断是否属于氧化物
⑤根据分散系的稳定性将分散系分为胶体、溶液和浊液.
| A. | 只有①②④ | B. | 只有③⑤ | C. | 只有④ | D. | 都不对 |
12.用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,33.6LSO3中含有原子数为6NA | |
| B. | 28g乙烯和环丁烷的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,2.24L氧气与足量镁粉充分反应,转移电子数为4NA | |
| D. | 117g氯化钠固体中含有2NA个氯化钠分子 |
18.${\;}_{55}^{137}$Cs是核反应堆的常见放射性副产物,${\;}_{55}^{137}$Cs能自发转化为${\;}_{56}^{137}$Ba,同时放出射线.下列有关叙述正确的是( )
| A. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba互为同位素 | |
| B. | ${\;}_{55}^{137}$Cs与${\;}_{56}^{137}$Ba中子数相等 | |
| C. | ${\;}_{56}^{137}$Ba原子最外层电子数为2 | |
| D. | Ba比Cs更容易失去电子 |