题目内容
18.下列物质中,含有金属键的是( )| A. | 干冰 | B. | 金刚石 | C. | 食盐 | D. | 白银 |
分析 A、干冰中存在共价键;
B、金刚石是原子晶体,存在共价键;
C、食盐是离子晶体存在离子键;
D、白银是金属晶体存金属键.
解答 解:A、干冰中存在共价键,而不含有金属键,故A错误;
B、金刚石是原子晶体,存在共价键,不含有金属键,故B错误;
C、食盐是离子晶体存在离子键,不含有金属键,故C错误;
D、白银是金属晶体存金属键,故D正确;
故选D.
点评 本题考查晶体类型的判断、晶体中的作用力、化学键等,难度不大,注意知识的积累.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
9.下列说法正确的是??( )
| A. | 麻黄碱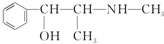 的催化氧化产物能发生银镜反应 的催化氧化产物能发生银镜反应 | |
| B. | 可用碘水和银氨溶液鉴别葡萄糖、麦芽糖和淀粉三种物质 | |
| C. | 油脂在人体内的化学变化主要是在脂肪酶的催化下进行水解 | |
| D. | 苯和油脂均不能使酸性高锰酸钾溶液褪色 |
9.下列各反应达到平衡后,减小压强或升高温度都能使化学平衡向正反应方向移动的是( )
| A. | N2(g)+3H2(g)?2NH3(g) (正反应为放热反应) | |
| B. | C(s)+CO2(g)?2CO(g) (正反应为吸热反应) | |
| C. | 2NO2(g)?N2O4(g) (正反应为放热反应) | |
| D. | 3O2(g)?2O3(g) (正反应为吸热反应) |
6.室温时,将足量的氯化银固体分别加入①10mL蒸馏水中;②30mL0.1mol/L盐酸;③5mL0.3mol/L食盐溶液;④10mL0.2mol/L氯化钙溶液中.均使氯化银溶解并达到饱和,此时所得各种溶液中,银离子浓度由大到小的顺序是( )
| A. | ①②③④ | B. | ①②④③ | C. | ①③②④ | D. | ④③①② |
13.下列装置能达到实验目的是( )
| A. | 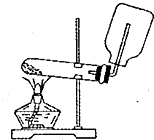 实验室制取并收集氨气 | B. | 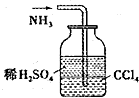 吸收氨气 | ||
| C. | 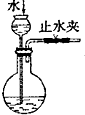 代替启普发生器 | D. | 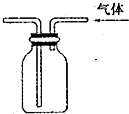 排空气法收集二氧化碳 |
3.主族元素R最高价氧化物对应水化物的化学式为H2RO3,则其氢化物的化学式是( )
| A. | HR | B. | RH3 | C. | H2R | D. | RH4 |
10.能得到Fe2O3 的实验是( )
| A. | 铁在纯氧中燃烧 | B. | 红热的铁和水蒸气反应 | ||
| C. | 蒸干并灼烧Fe2(SO4)3溶液 | D. | 灼烧氢氧化铁固体 |
8.下列说法中错误的是( )
| A. | 位于 IA的元素与位于ⅦA的元素组成的化合物都是离子化合物 | |
| B. | 元素周期表中ⅡA族的元素都是金属元素 | |
| C. | 元素周期表有7个横行,18个纵列 | |
| D. | 除氦外的稀有气体原子的最外层电子数都是8个 |