题目内容
17.用短线“-”表示共用电子对,用“‥”表示未成键孤对电子的式子叫路易斯结构式.以下路易斯结构式表示的分子属极性分子的是( )①

②

③

④

| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ③④ |
分析 由非极性键构成的分子,一定为非极性分子;而由极性键构成的分子,若结构对称,正负电荷的中心重合,则为非极性分子,据此分析.
解答 解:根据路易斯结构式可知,① 为CO2,在二氧化碳中,碳氧键为极性键,但由于二氧化碳中两条碳氧键对称,故极性抵消,正负电荷中心重合,故为非极性分子;
为CO2,在二氧化碳中,碳氧键为极性键,但由于二氧化碳中两条碳氧键对称,故极性抵消,正负电荷中心重合,故为非极性分子;
② 中三条键均为极性键,但由于其结构对称,三条键的极性能相互抵消,故为非极性分子;
中三条键均为极性键,但由于其结构对称,三条键的极性能相互抵消,故为非极性分子;
③ 为NH3或PH3,结构中三条键均为极性键,但由于三条键的极性不能相互抵消,故为极性分子;
为NH3或PH3,结构中三条键均为极性键,但由于三条键的极性不能相互抵消,故为极性分子;
④ 为H2O或H2S,结构中两条键均为极性键,但由于两条键的极性不能相互抵消,故为极性分子;
为H2O或H2S,结构中两条键均为极性键,但由于两条键的极性不能相互抵消,故为极性分子;
故选D.
点评 本题考查了键的极性和分子极性之间的关系,应注意的是由极性键构成的是不是极性分子取决于分子的空间构型.

练习册系列答案
相关题目
6.下列物质中,既有离子键又有共价键的是( )
| A. | CaCl2 | B. | KOH | C. | NH3•H2O | D. | H2SO4 |
20.某化学小组用如图装置做兴趣实验(具支试管中存有少量空气).
完成下列填空:
(1)实验1:同时加入试剂,反应开始可观察到U形管中液面b(填字母,下同),反应结束静置一段时间,最终U形管中液面c.
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后,U形管中液面出现左低右高,则b管中发生反应的氧化剂是O2(填化学式).
(3)实验3:一段时间后,红棕色气体在b(填“a”或“b”)管液面上方出现,简述另外一试管未出现任何现象的原因:铝在浓硝酸中发生钝化.在其他条件不变的情况下,若将a、b试管中浓硝酸同时改为3mLcd(填编号),即可观察到试管中产生无色的气体,且位置与上述是相反的.
a.无水乙醇 b.浓硫酸 c.稀硫酸 d.烧碱溶液
(4)实验4:一段时间后,U形管中的液面情况是左高右低(用文字简述);写出a试管中发生还原反应的电极反应式:O2+2H2O+4e-═4OH-.
| 实验编号 | a中试剂 | b中试剂 | 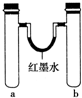 |
| 1 | 0.1g Na、3mL水 | 0.1g Na、3mL乙醇 | |
| 2 | 3mL水 | 3mL饱和FeSO4溶液 | |
| 3 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 | |
| 4 | 生铁钉、3mL饱和食盐水 | 生铁钉、3mL饱和氯化铵溶液 |
(1)实验1:同时加入试剂,反应开始可观察到U形管中液面b(填字母,下同),反应结束静置一段时间,最终U形管中液面c.
a.左高右低 b.左低右高 c.左右基本持平
(2)实验2:一段时间后,U形管中液面出现左低右高,则b管中发生反应的氧化剂是O2(填化学式).
(3)实验3:一段时间后,红棕色气体在b(填“a”或“b”)管液面上方出现,简述另外一试管未出现任何现象的原因:铝在浓硝酸中发生钝化.在其他条件不变的情况下,若将a、b试管中浓硝酸同时改为3mLcd(填编号),即可观察到试管中产生无色的气体,且位置与上述是相反的.
a.无水乙醇 b.浓硫酸 c.稀硫酸 d.烧碱溶液
(4)实验4:一段时间后,U形管中的液面情况是左高右低(用文字简述);写出a试管中发生还原反应的电极反应式:O2+2H2O+4e-═4OH-.
8.钾的金属活动性比钠强,根本原因( )
| A. | 钾的密度比钠小 | B. | 钾的熔点比钠低 | ||
| C. | 钾原子比钠原子多一个电子层 | D. | 加热时钾比钠更易汽化 |
5.为证明化学反应有一定的限度,进行如下探究活动:I.取5m1 0.1mol/L的KI溶液,滴加几滴FeCl3稀溶液(已知:2Fe3++2I-=I2+2Fe2+)Ⅱ.继续加入2ml CCl4振荡.Ⅲ.取萃取后的上层清液,滴加KSCN溶液.
(1)探究活动I的实验现象为溶液呈棕黄色;探究活动Ⅱ的实验现象为溶液分层,下层CCl4层呈紫红色.
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+;
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大,Fe(SCN)3在乙醚中与在水中呈现的颜色相同;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6](黄色)溶液检验Fe3+的灵敏度比用KSCN更高.结合新信息,现设计以下实验方案验证猜想:
ⅰ.请完成下表实验操作、现象和结论
ⅱ.写出实验操作“步骤一”中反应的离子方程式为4Fe3++3[Fe(CN)6]4-═Fe4[Fe(CN)6]3↓..
(1)探究活动I的实验现象为溶液呈棕黄色;探究活动Ⅱ的实验现象为溶液分层,下层CCl4层呈紫红色.
(2)探究活动Ⅲ的意图是通过生成血红色的Fe(SCN)3溶液,验证有Fe3+残留,从而证明化学反应有一定的限度,但在实验中却未见溶液呈血红色.对此同学们提出了下列两种猜想:
猜想一:Fe3+全部转化为Fe2+;
猜想二:生成的Fe(SCN)3浓度极小,其颜色肉眼无法观察.
为了验证猜想,查阅资料获得下列信息:
信息一:乙醚微溶于水,Fe(SCN)3在乙醚中的溶解度比在水中大,Fe(SCN)3在乙醚中与在水中呈现的颜色相同;
信息二:Fe3+可与[Fe(CN)6]4-反应生成蓝色沉淀,用K4[Fe(CN)6](黄色)溶液检验Fe3+的灵敏度比用KSCN更高.结合新信息,现设计以下实验方案验证猜想:
ⅰ.请完成下表实验操作、现象和结论
| 实 验 操 作 | 现 象 和 结 论 |
| 步骤一:取萃取后的上层清液滴加2滴K4[Fe(CN)6] | 若产生①蓝色沉淀, 则②猜想一不成立; |
| 步骤二:往探究Ⅲ所得溶液中加入少量乙醚,充分振荡、静置分层 | 若③乙醚层呈血红色, 则④猜想二成立; |
12.某些保健品中含有的锗元素(Ge)位于周期表的第四周期IVA族.有关锗的叙述不正确的是( )
| A. | 锗的原子序数为24 | B. | 锗的金属活动性应比硅强 | ||
| C. | Ge可以生成化学式为Na2GeO3的盐 | D. | 单质锗是半导体材料 |
2.下列文字表述与反应方程式对应,且正确的是( )
| A. | 用醋酸除去水垢:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| B. | 利用腐蚀法制作印刷线路板:Fe3++Cu=Fe2++Cu2+ | |
| C. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓ | |
| D. | 用液溴和苯在催化剂作用下制溴苯: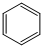 +Br2$\stackrel{催化剂}{→}$ +Br2$\stackrel{催化剂}{→}$ +HBr +HBr |
9.下列关于氯化氢的叙述中,正确的是( )
| A. | 氯化氢是白色有刺激性气味的气体 | |
| B. | 氯化氢具有强酸性 | |
| C. | 氯化氢能使干燥的蓝色石蕊试纸变红 | |
| D. | 氯化氢极易溶于水 |