题目内容
分类是科学研究的重要依据,下列物质分类不正确的是( )
| A、混合物:铝热剂、液氨、水玻璃、明矾 |
| B、化合物:干冰、冰水混合物、烧碱、小苏打 |
| C、电解质:氯化钠、硫酸钡、氯化氢、水 |
| D、同素异形体:活性炭、C60、石墨烯、金刚石 |
考点:混合物和纯净物,同素异形体,单质和化合物,电解质与非电解质
专题:物质的分类专题
分析:A、混合物是不同物质组成的物质;
B、化合物是不同元素组成的纯净物;
C、电解质是水溶液中或熔融状态下能导电的化合物;
D、依据同素异形体概念是同种元素组成的不同单质分析判断.
B、化合物是不同元素组成的纯净物;
C、电解质是水溶液中或熔融状态下能导电的化合物;
D、依据同素异形体概念是同种元素组成的不同单质分析判断.
解答:
解:A、铝热剂是铝和金属氧化物的混合物、液氨是液体氨气属于纯净物、水玻璃是硅酸钠的水溶液属于混合物、明矾属于盐是纯净物,故A错误;
B、干冰是二氧化碳、烧碱是氢氧化钠、冰水混合物是水、小苏打属于纯净的化合物,故B正确;
C、氯化钠是盐属于电解质,硫酸钡是盐属于电解质,氯化氢水溶液中导电是电解质,水是弱电解质,故C正确;
D、活性炭、C60、石墨烯、金刚石都是碳元素组成的纯净物属于单质,结构不同,物理性质不同属于同素异形体,故D正确;
故选A.
B、干冰是二氧化碳、烧碱是氢氧化钠、冰水混合物是水、小苏打属于纯净的化合物,故B正确;
C、氯化钠是盐属于电解质,硫酸钡是盐属于电解质,氯化氢水溶液中导电是电解质,水是弱电解质,故C正确;
D、活性炭、C60、石墨烯、金刚石都是碳元素组成的纯净物属于单质,结构不同,物理性质不同属于同素异形体,故D正确;
故选A.
点评:本题考查了化学概念和物质分类的分析判断,掌握实质是解题关键,题目较简单.

练习册系列答案
相关题目
下列物质中属于强电解质的是( )
| A、盐酸 |
| B、BaSO4 |
| C、CH3COONa |
| D、H2O |
下列说法正确的是( )
| A、工业合成氨反应使用催化剂,加快化学反应速率,并提高产率,增大经济效益 |
| B、水的离子积常数Kw只与温度有关,但加酸、碱、盐一定会影响水的电离程度 |
| C、等物质的量浓度,等体积的NaCl溶液和NaClO溶液中离子数目前者大于后者 |
| D、将等PH的盐酸溶液和醋酸溶液稀释相同的倍数,稀释后PH:盐酸<醋酸 |
下列物质的水溶液中存在溶质分子的是( )
| A、HCl |
| B、NaOH |
| C、Na2CO3 |
| D、酒精 |
制备氰氨化钙的化学方程式为CaCO3+2HCN═CaCN2+CO↑+H2↑+CO2↑,在反应中( )
①氢元素被氧化,碳元素被还原
②HCN既是氧化剂又是还原剂
③CaCN2是氧化产物,H2是还原产物
④CO为氧化产物,H2为还原产物.
①氢元素被氧化,碳元素被还原
②HCN既是氧化剂又是还原剂
③CaCN2是氧化产物,H2是还原产物
④CO为氧化产物,H2为还原产物.
| A、①② | B、③④ | C、①④ | D、②③ |
25℃时,甲、乙、丙三个烧杯分别盛有25mL、浓度均为0.10mol?L-1的醋酸、氢氧化钠溶液和醋酸钠溶液.下列说法正确的是( )
| A、乙溶液和丙溶液混合后,Na+浓度仍为0.10mol?L-1 |
| B、甲溶液和乙溶液混合后所得溶液的pH和丙溶液相同 |
| C、若甲与丙两溶液混合后溶液显酸性,则c(CH3COO-)-c(CH3COOH)=c(H+)-c(OH-) |
| D、将丙溶液加到甲溶液中,则CH3COOH的电离平衡常数Ka变小 |
下列说法不正确的是( )
| A、C2H4和HCN分子中,都含σ键和π键,但C原子的杂化方式并不相同 |
| B、在元素周期表中,p区元素的最外层电子排布均可表示为ns2np1~6 |
C、某基态原子的核外电子排布图为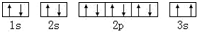 ,它违背了泡利不相容原理 ,它违背了泡利不相容原理 |
| D、用红外光谱可鉴别乙醇和二甲醚,用X-射线衍射实验可鉴别玻璃与水晶 |
四种仪器中,不能用来加热的是( )
A、 烧杯 |
B、 容量瓶 |
C、 试管 |
D、 烧瓶 |