题目内容
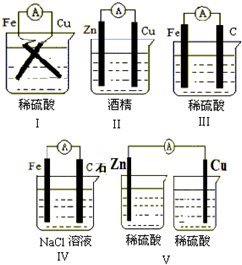
下列装置能否组成原电池?并判断正负极.

考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,只要符合原电池构成条件即可形成原电池.
解答:
解:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,只要符合原电池构成条件即可形成原电池.
Ⅰ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅱ、酒精不是电解质,所以不能组成原电池;
Ⅲ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅳ、符合构成原电池的基本条件,能够组成原电池(类似于金属的吸氧腐蚀),负极为较活泼金属Fe;
Ⅴ、不能够形成闭合回路,所以不能组成原电池,
答:Ⅰ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅱ、酒精不是电解质,所以不能组成原电池;
Ⅲ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅳ、符合构成原电池的基本条件,能够组成原电池(类似于金属的吸氧腐蚀),负极为较活泼金属Fe;
Ⅴ、不能够形成闭合回路,所以不能组成原电池.
Ⅰ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅱ、酒精不是电解质,所以不能组成原电池;
Ⅲ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅳ、符合构成原电池的基本条件,能够组成原电池(类似于金属的吸氧腐蚀),负极为较活泼金属Fe;
Ⅴ、不能够形成闭合回路,所以不能组成原电池,
答:Ⅰ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅱ、酒精不是电解质,所以不能组成原电池;
Ⅲ、符合构成原电池的基本条件,能够组成原电池,负极为较活泼金属Fe;
Ⅳ、符合构成原电池的基本条件,能够组成原电池(类似于金属的吸氧腐蚀),负极为较活泼金属Fe;
Ⅴ、不能够形成闭合回路,所以不能组成原电池.
点评:本题以原电池原理为载体考查了原电池的构成条件,难度不大,根据原电池构成条件来分析解答即可.

练习册系列答案
相关题目
次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐(不存在酸式盐).下列叙述中正确的是( )
| A、次磷酸(H3PO2)是三元酸 |
| B、H3PO2中磷为+1价 |
| C、NaH2PO2溶液呈酸性 |
| D、次磷酸根离子为-3价 |
根据原子结构及元素周期律的知识,下列推断正确的是( )
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| B、核外电子排布相同的微粒化学性质也相同 | ||||
| C、S2?、Cl?、K+、Ca2+半径逐渐减小 | ||||
D、
|
实验室制氮气,可用NaO2晶体与NH4Cl饱和溶液在加热的条件下发生如下反应:NaNO2+NH4Cl
NaCl+2H2O+N2↑,下列关于该反应的说法正确的是( )
| ||
| A、NaNO2是还原剂 |
| B、NH4Cl是氧化剂 |
| C、反应中有离子键、极性共价键和非极性共价键的断裂和形成 |
| D、每生成lmolN2,NaNO2得到3mol电子 |